Wzorcowanie i adiustacja (część 3)
Autorzy: Dr Markus Schubnell, Dr Domenico Regonini
Stabilność oksydacyjna olejów, tłuszczów lub polimerów jest często charakteryzowana poprzez określenie czasu indukcji utleniania (OIT). W niniejszym artykule opisujemy procedurę analityczną oraz omawiamy czynniki wpływające na mierzone OIT.
Wstęp
Stabilność oksydacyjna olejów, tłuszczów lub polimerów jest często charakteryzowana poprzez wykonywanie tzw. pomiarów OIT (czas indukcji utleniania). W metodzie tej próbka jest najpierw podgrzewana do określonej temperatury w warunkach obojętnych (zazwyczaj w atmosferze azotu). Po krótkiej fazie stabilizacji w tej temperaturze (i nadal w warunkach obojętnych), cela DSC jest przedmuchiwana tlenem lub powietrzem. Następnie, po pewnym czasie, sygnał DSC pokazuje wzrost przepływu ciepła w kierunku egzotermicznym. Czas do początku tego procesu jest znany jako czas indukcji utleniania lub OIT (ang. Oxidation induction time). Szczegóły dotyczące procedury są opisane w różnych normach (np. ASTM D 4065 (poliolefiny), ASTM E 1858 (węglowodory), ISO EN DIN 11357-6). Przed właściwym pomiarem OIT często określana jest temperatura onset dla utleniania próbki (ang. Oxidation onset temperature; OOT) w celu uzyskania informacji o temperaturze najbardziej odpowiedniej do pomiaru OIT. OOT wyznacza się w eksperymencie grzewczym (szybkość grzania to zazwyczaj 10 K/min) z wykorzystaniem tego samego gazu w celi, który ma być użyty w następnym pomiarze OIT (powietrze lub czysty tlen). Temperaturę, która sprawia, że OIT nie jest ani zbyt długie ani zbyt krótkie, uzyskuje się przez odjęcie 30 do 40 K od OOT (to oczywiście zależy od szybkości grzania użytej do pomiaru OOT).
Szczegóły eksperymentu
Pomiary przeprowadzono przy pomocy DSC z czujnikiem FRS6 oraz intracoolerem. DSC uprzednio starannie wykalibrowano i dokonano jego adiustacji, stosując metody omówione w [1]. Wyniki niemal izotermicznych pomiarów kalibracyjnych dla indu i cyny zestawiono w tabeli 1.
Tabela 1. Wyniki niemal izotermicznych pomiarów kalibracyjnych z indem i cyną.
|
Materiał referencyjny |
Temperatura topnienia (zmierzona) |
Temperatura topnienia (literatura) |
|
Ind (In) |
156,6 °C |
156,6 °C |
|
Cyna (Sn) |
231,7 °C |
231,9 °C |
Próbki były najpierw ogrzewane w powietrzu z prędkością 10 K/min przy przepływie 50 ml/min w celu wyznaczenia OOT. W zależności od konkretnej OOT, dla każdej próbki zdefiniowano pięć temperatur, w których mierzono OIT. Pomiary OIT przeprowadzono w następujący sposób: ogrzewanie w azocie do temperatury docelowej OIT z prędkością 10 K/min, stabilizacja próbek w temperaturze docelowej w azocie przez 5 min, a następnie pomiar OIT w tej samej temperaturze w atmosferze powietrza przy 50 ml/min. Masa próbki za każdym razem wynosiła około 3 mg. Jak zwykle w przypadku OIT/OOT, próbki były mierzone w otwartych tyglach aluminiowych o pojemności 40 μl.
Zależność OIT polimerów od temperatury
W dziedzinie polimerów, pomiary OIT są bardzo często wykonywane dla poliolefin (najważniejsze produkty to: polietylen, polipropylen). Na rysunku 1 lewa strona wykresu przedstawia krzywe OIT polipropylenu mierzone w różnych temperaturach w powietrzu przy przepływie 50 ml/min. Dla jasności oś czasu przedstawiono w skali logarytmicznej; ocenę OIT przeprowadzono jednak w liniowej skali czasu. Górna krzywa po prawej stronie rysunku 1 przedstawia pomiar OOT przy 10 K/min również w powietrzu przy 50 ml/min. Pik endotermiczny od około 155°C jest spowodowany topnieniem próbki. Wykres w prawej dolnej części rysunku 1 przedstawia zależność OIT próbki polipropylenu od temperatury. Wynika z tego, że OIT silnie zależy od temperatury. Dlatego bardzo ważna jest staranna kalibracja DSC przy użyciu niemal izotermicznych metod kalibracji. Szczegóły, jak to zrobić, można znaleźć w [1]. Polimery różnią się znacznie od siebie pod względem składu chemicznego i struktury i nie wszystkie z nich mogą być scharakteryzowane pod względem stabilności termicznej za pomocą OIT. W porównaniu z polimerami, tłuszcze i oleje roślinne są znacznie bardziej podobne do siebie. W dalszej części rozdziału omówimy bardziej szczegółowo pomiary OIT i OOT dla tłuszczów i olejów roślinnych.
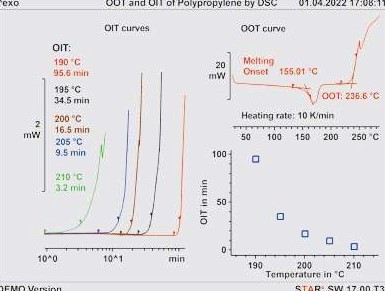
Rysunek 1. Łącza: krzywe pomiarowe OIT dla polipropylenu w różnych temperaturach. Po prawej stronie: krzywa pomiaru OOT (powyżej) i zależność OIT od temperatury (poniżej).
OIT i OOT tłuszczów i olejów roślinnych
Tłuszcze i oleje roślinne składają się głównie z triglicerydów. Powstają one w wyniku estryfikacji glicerolu z trzema kwasami tłuszczowymi. Kwas tłuszczowe mogą różnić się długością łańcucha. Ogólną strukturę triglicerydu przedstawiono na rysunku 2.
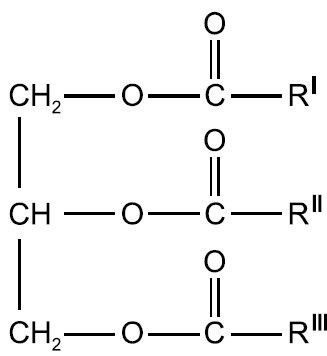
Rysunek 2. Ogólna budowa triglicerydu
Produkty naturalne składają się z mieszanin różnych triglicerydów z różnymi estrami kwasów tłuszczowych (R’, R”, R’”). Atomy węgla w łańcuchach kwasów tłuszczowych są połączone ze sobą wiązaniami pojedynczymi lub podwójnymi. Jeśli nie występują wiązania podwójne, tłuszcz (lub olej) jest określany jako „nasycony”, a w przeciwnym razie jako „nienasycony”1). Kwasy tłuszczowe w olejach charakteryzują się dwoma liczbami. Pierwsza liczba odnosi się do liczby atomów węgla, druga do liczby wiązań podwójnych. Nasycone triglicerydy mają wyższe temperatury topnienia niż odpowiadające im nienasycone triglicerydy. Ponadto, temperatura topnienia wzrasta wraz ze wzrostem długości łańcucha kwasu tłuszczowego. Nienasycone kwasy tłuszczowe są mniej stabilne termicznie. Oleje wymienione w tabeli 2 zostały zbadane pod kątem ich OIT. Olej palmow y jest dostępny w różnych formach: jako olej palmowy, olej z ziaren palmowych i uwodorniony olej palmowy. Olej palmowy i olej z ziaren palmowych są otrzymywane z różnych części owoców palmy oleistej (olej palmowy z miąższu owoców palmy, olej z ziaren palmowych (nasion)). Skład oleju palmowego i oleju z ziaren palmowych różni się m.in. stopniem nasycenia kwasów tłuszczowych – zawartość nasyconych kwasów tłuszczowych w oleju palmowym wynosi ok. 45%, a w oleju z ziaren palmowych ok. 83%. W badanym przez nas uwodornionym oleju palmowym (produkt przemysłowy stosowany również jako „bio-dodatek” do oleju napędowego) zawartość nasyconych kwasów tłuszczowych wynosiła około 90%. Tabela 3 przedstawia zawartość nasyconych i nienasyconych kwasów tłuszczowych w różnych badanych przez nas olejach.
Tabela 2. Najważniejsze kwasy tłuszczowe i ich zawartość w różnych olejach [2]; FA: kwas tłuszczowy.
|
Oliwa z oliwek |
Olej słonecznikowy |
Olej kokosowy |
Olej palmowy (uwodorniony) |
Olej lniany
|
|||||
|
FA |
Zawartość |
FA |
Zawartość |
FA |
Zawartość |
FA |
Zawartość |
FA |
Zawartość
|
|
16:0 |
9–15% |
16:0 |
4–10% |
12:0 |
40–50% |
16:0 |
35–45% |
18:1 |
15–20% |
|
18:1 |
65–85% |
18:1 |
20–30% |
14:0 |
15–20% |
18:0 |
40–50% |
18:2 |
15–20% |
|
18:2 |
5–15% |
18:2 |
55–65% |
16:0 |
8 –10% |
18:1 |
5–12% |
18:3 |
45–55% |
Tabela 3. Typowe zawartości nasyconych i nienasyconych kwasów tłuszczowych w różnych olejach [2].
|
|
Oliwa z oliwek
|
Olej słonecznikowy
|
Olej kokosowy
|
Olej palmowy (uwodorniony)
|
Olej lniany
|
|
Nasycone |
15% |
10% |
84% |
90% |
6% |
|
Jednonienasycone |
75% |
30% |
7% |
7% |
17% |
|
Wielonienasycone |
10% |
60% |
9% |
3% |
77% |
Zależność OIT od temperatury
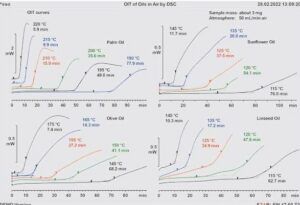
Rysunek 3. Krzywe DSC-OIT przedstawiające izotermiczny rozkład oksydacyjny różnych olejów w kilku różnych temperaturach w powietrzu przy przepływie 50 ml/min.
Przykładowo, na rysunku 3 przedstawiono krzywe DSC-OIT dla kilku olejów mierzone w różnych temperaturach izotermicznych w powietrzu jako gazem metody przy przepływie 50 ml/min. Zgodnie z oczekiwaniami OIT zmniejsza się wraz ze wzrostem temperatury. Ponadto egzotermiczny strumień ciepła wytwarzany podczas utleniania olejów wzrasta szybciej w wyższych temperaturach. Oznacza to, że rozkład oksydacyjny olejów następuje szybciej w wyższych temperaturach. Na rysunku 4 przedstawiono temperaturową zależność OIT dla olejów z rysunku 3. Zależność OIT od temperatury można opisać za pomocą funkcji Arrheniusa zgodnie ze wzorem 1:
OIT = α· e –Ea /(R ·T) (wzór 1)
Tutaj T jest temperaturą w K, Ea energią aktywacji (w J/mol), R stałą gazową R=8,314 J/(mol K), i α , w tym przypadku, jest nieistotnym czynnikiem wstępnym.
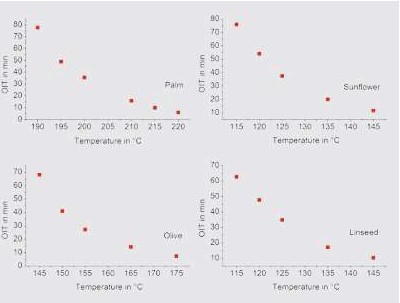
Rysunek 4. Zależność OIT od temperatury dla różnych olejów.
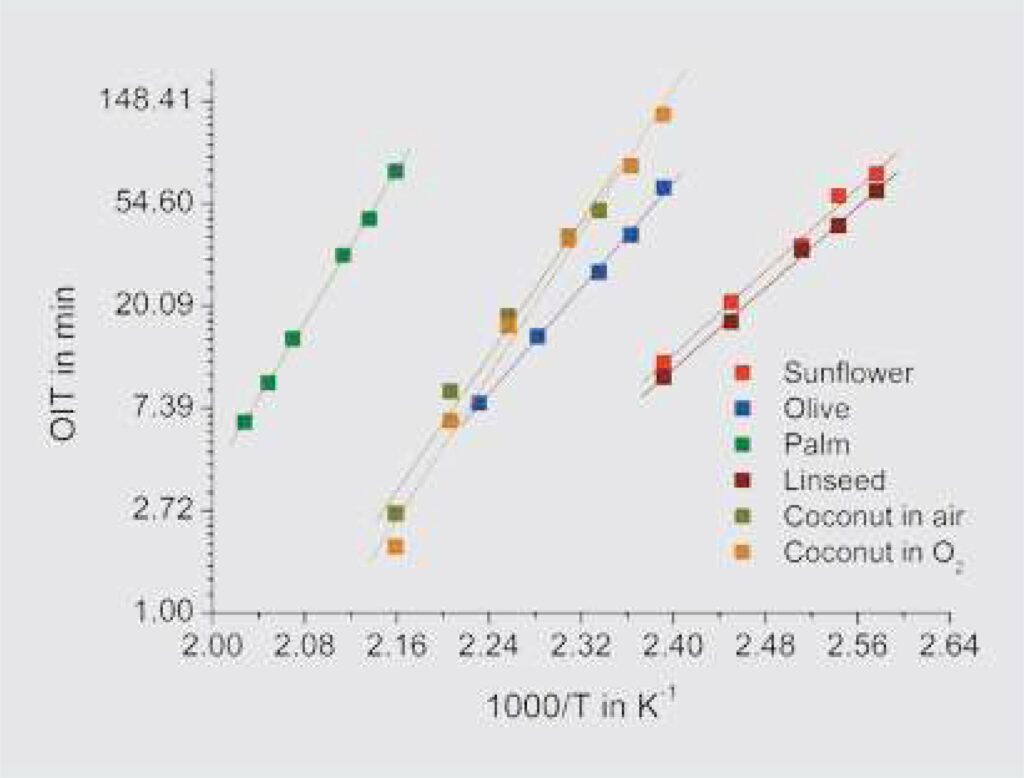
Rysunek 5. OIT dla mierzonych przez nas olejów w różnych temperaturach.
Jak pokazano na rysunku 5, OIT wykreślone w skali logarytmicznej jako odwrotna funkcja temperatury daje, zgodnie ze wzorem 1, liniową zależność pomiędzy OIT i temperaturą wzajemną. Linie ciągłe na rysunku 5 odpowiadają „najlepszym dopasowaniom” dla różnych olejów. Energię aktywacji reakcji utleniania można obliczyć na podstawie nachylenia linii ,m, zgodnie ze wzorem 2:
Ea = m · R (wzór 2).
Wyniki wskazują, że temperaturową zależność OIT dla olejów można opisać za pomocą wzoru 1 (współczynnik korelacji dla wszystkich olejów > 0,98). Największe odchylenia stwierdzono w oleju kokosowym. Olej kokosowy składa się głównie z krótkołańcuchowych nasyconych kwasów tłuszczowych, które ulegają tylko powolnemu rozkładowi oksydacyjnemu w powietrzu. Utrudnia to określenie OIT w powietrzu. Z tego powodu OIT dla oleju kokosowego oznaczono również w czystym tlenie. W czystym tlenie, OIT w danej temperaturze są na ogół krótsze niż w powietrzu. „Egzotermiczny” wzrost przepływu ciepła jest również znacznie szybszy, co sprawia, że określenie OIT w tlenie w porównaniu z powietrzem jest łatwiejsze i bardziej precyzyjne. Począwszy od około 150°C rozkład oksydacyjny oleju kokosowego w powietrzu jest tak powolny, że nie można już określić OIT. W czystym tlenie jest to możliwe nawet w niższych temperaturach. Pomiary OIT oleju kokosowego w powietrzu (krzywe przerywane) i w tlenie (krzywe ciągłe) przedstawiono na rysunku 6.
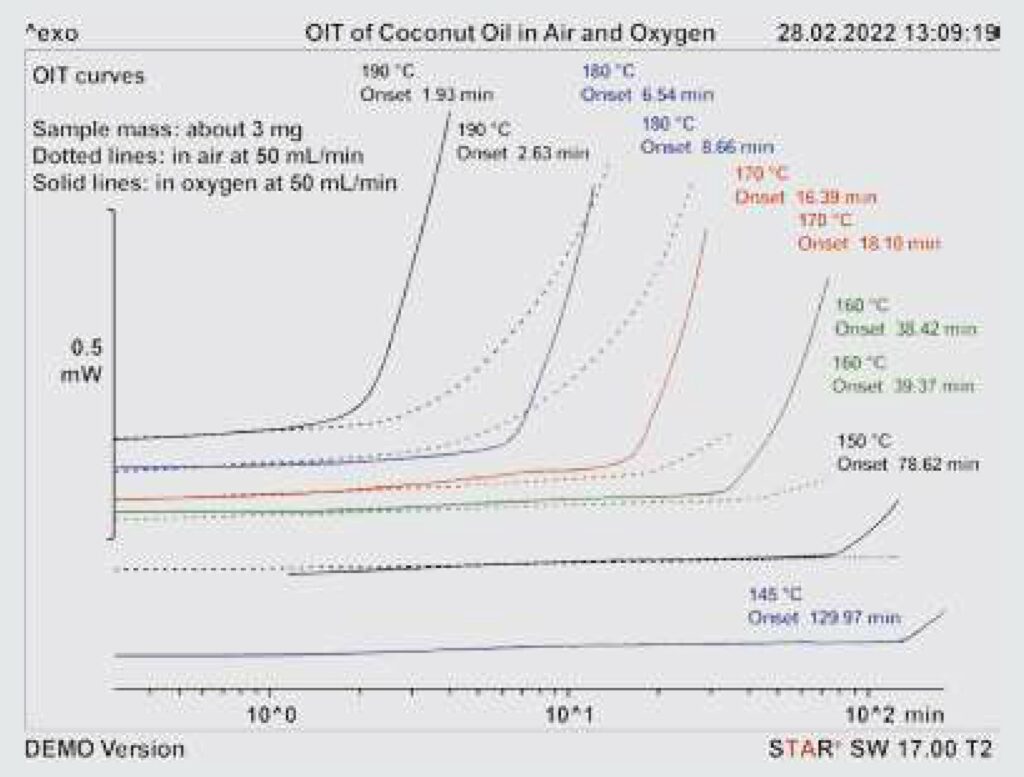
Rysunek 6. Krzywe OIT oleju kokosowego mierzone w tlenie (linie ciągłe) i w powietrzu (linie przerywane). Szczegóły w tekście.
Dla przejrzystości, oś czasu przedstawiono w formie logarytmicznej. OIT były wyznaczane na liniowej osi czasu. Rysunek 5 pokazuje również, że OIT oleju lnianego różnią się tylko nieznacznie od OIT oleju słonecznikowego. Nie jest to szczególnie zaskakujące, ponieważ skład obydwu olejów jest dość podobny (patrz tabele 2 i 3). Główna różnica wynika z dużej ilości nienasyconych kwasów tłuszczowych z trzema podwójnymi wiązaniami (zwanych również kwasami tłuszczowymi omega-3) w oleju lnianym. W porównaniu z olejem słonecznikowym, dla oleju lnianego oczekuje się nieco krótszych OIT.
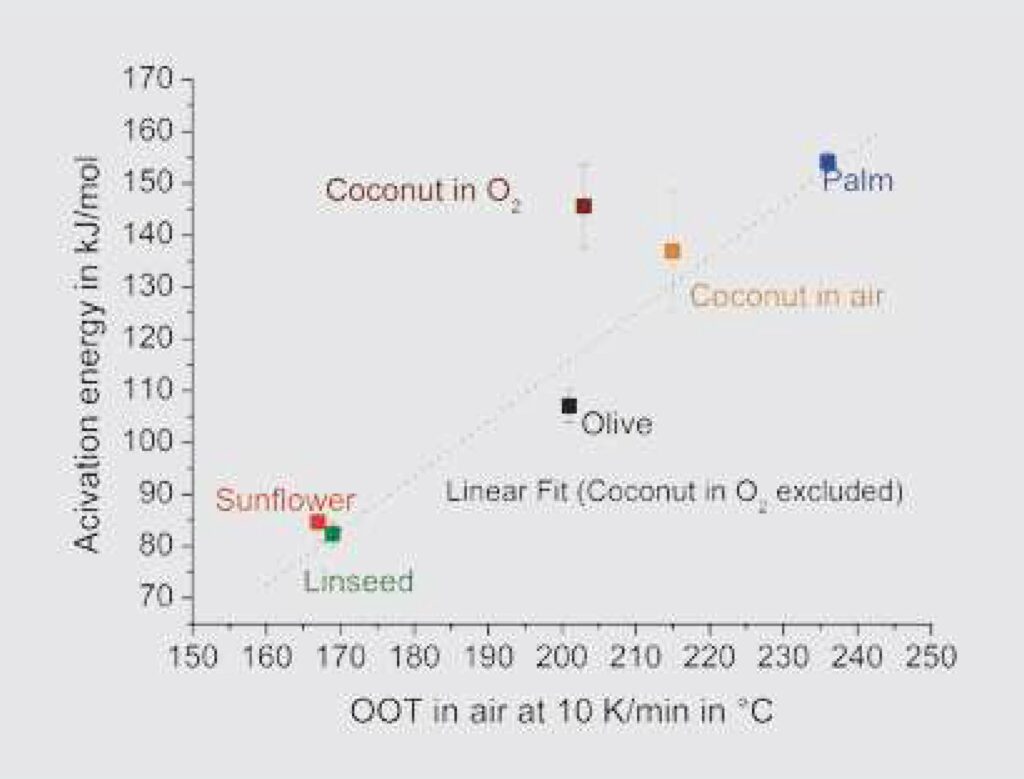
Rysunek 7. Energia aktywacji dla rozkładu oksydacyjnego różnych olejów wykreślona w funkcji OOT, mierzona przy 10 K/min w powietrzu. Punkt pomiarowy dla oleju kokosowego w tlenie nie był brany pod uwagę przy dopasowaniu liniowym.
Obliczone wartości energii aktywacji dla utleniania zmierzonych olejów przedstawiono na rysunku 7 w funkcji OOT (wyznaczonej na podstawie pomiarów w powietrzu przy 10 K/min). Wyniki wskazują na liniową zależność pomiędzy tymi dwoma wielkościami (współczynnik korelacji 0,992). Energia aktywacji dla utleniania oleju kokosowego w tlenie nie była brana pod uwagę przy obliczaniu „najlepszego dopasowania” linii kropkowanej. Pomiary OOT w powietrzu przedstawiono na rysunku 8.
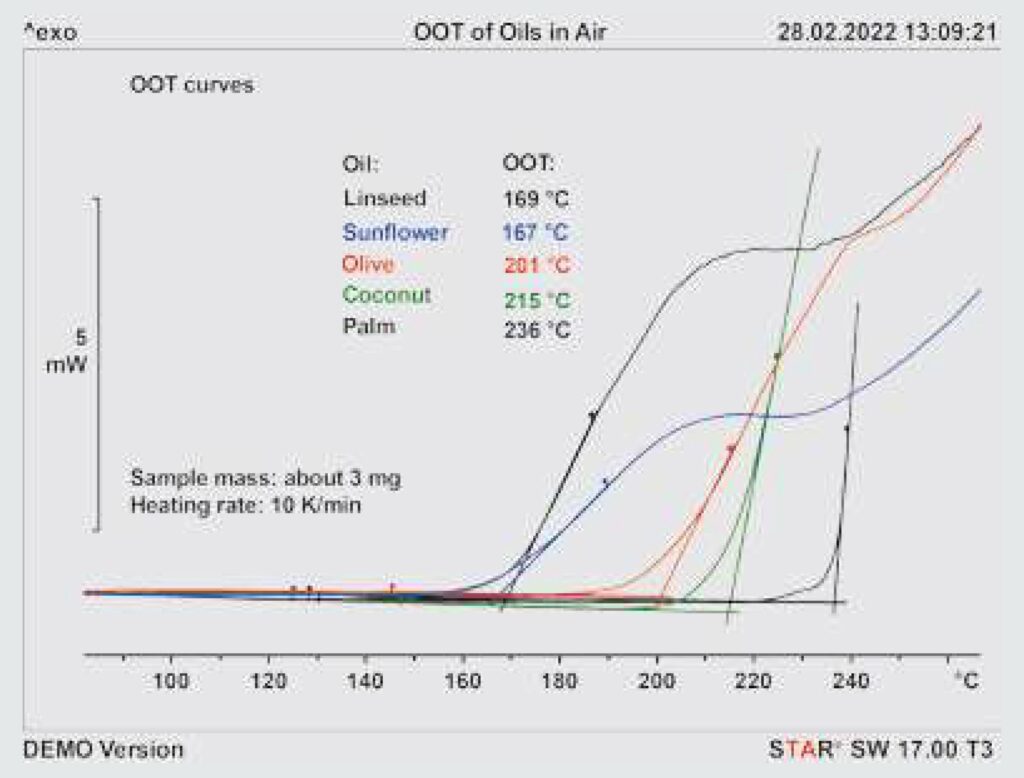
Rysunek 8. OOT dla pięciu badanych olejów, mierzone przy 10 K/min w powietrzu przy 50 ml/min; masa próbki wynosiła ok. 3 mg.
Aby oszacować wpływ temperatury na OIT, obliczono pierwsze pochodne OIT od krzywych T-1 (krzywe ciągłe na rysunku 5, wzór 1) dla olejów przy odpowiednich OIT, następnie znormalizowano do OIT odpowiadających tym temperaturom i wykreślono jako funkcję zmierzonych OIT. Jak wynika z rysunku 9, procentowy wpływ temperatury na OIT określony w ten sposób dla pięciu olejów jest z dobrym przybliżeniem niezależny od oleju i OIT. Daje to średnią wartość dla wszystkich OIT mierzonych w powietrzu wynoszącą (7,3 ± 1,2) %/K. Wartość tą można przyjąć jako praktyczną zasadę: niepewność temperatury o 1 K zmienia OIT mierzony w powietrzu o ±7,3%. W DSC ustawionym zgodnie z procedurą podaną w [1] spodziewamy się maksymalnej niepewności temperatury ±0,2 K (patrz również tabela 1). Oznacza to, że niepewność temperatury skutkuje niepewnością (odchyleniem standardowym) OIT wynoszącą około 1,5%. Z drugiej strony, na przykład, oznacza to, że systematyczne odchylenie temperatury o 2 K spowodowane nieprawidłową adiustacją prowadzi do błędu wynoszącego prawie 15% w zmierzonym OIT. Staranna izotermiczna adiustacja temperatury jest zatem niezbędna dla dokładnych pomiarów OIT. Oprócz temperatury, wpływ na dokładność oznaczenia wartości OIT ma przygotowanie próbki i oznaczanie OIT (granice oceny). Konieczne są zatem dalsze badania w celu poznania tych dwóch czynników. Jako przykład przedstawiamy możliwe podejścia w przypadku oleju palmowego. Wykres po lewej stronie na rysunku 10 przedstawia tą samą krzywą OIT dla próbki oleju palmowego (mierzoną w powietrzu w temperaturze 200°C) ocenianą pięciokrotnie, ale za każdym razem z nieco innymi wartościami granicznymi oceny. Numerycznie daje to średnią OIT wynoszącą 24,09 min i odchylenie standardowe 0,09 min. Udział w niepewności OIT oleju palmowego wynikający z tej oceny jest bardzo mały i może być pominięty.
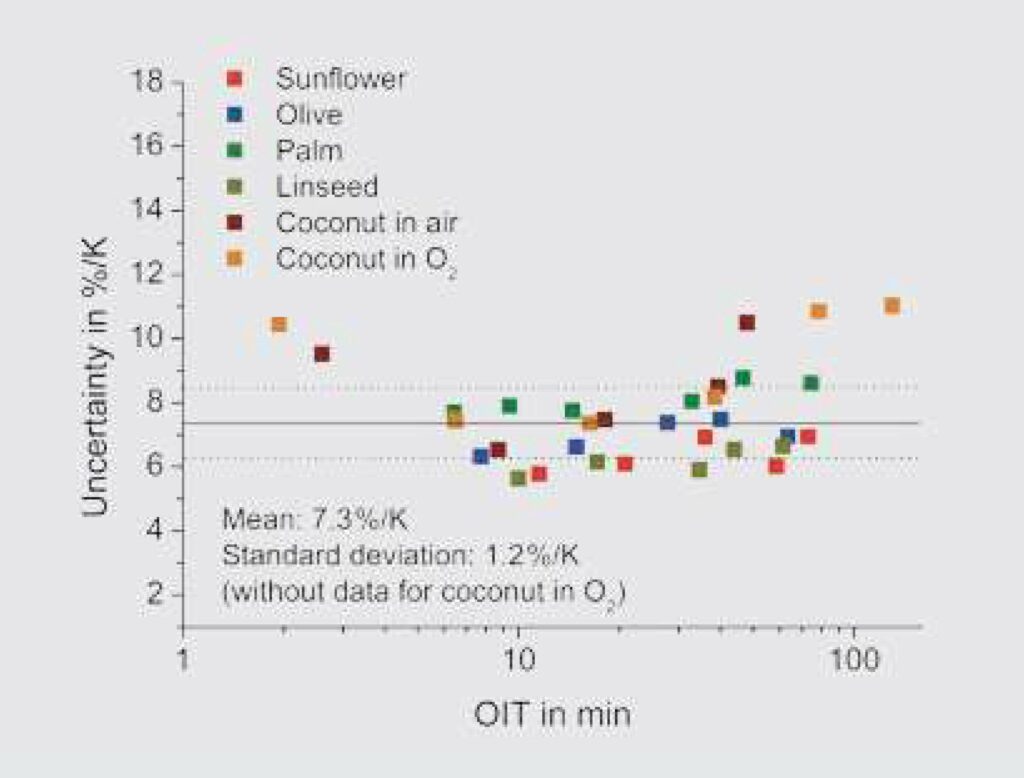
Rysunek 9. Wpływ temperatury na niepewność pomiarów OIT olejów. Z reguły niepewność temperatury 1 K oznacza niepewność około 7,3% dla OIT w powietrzu.
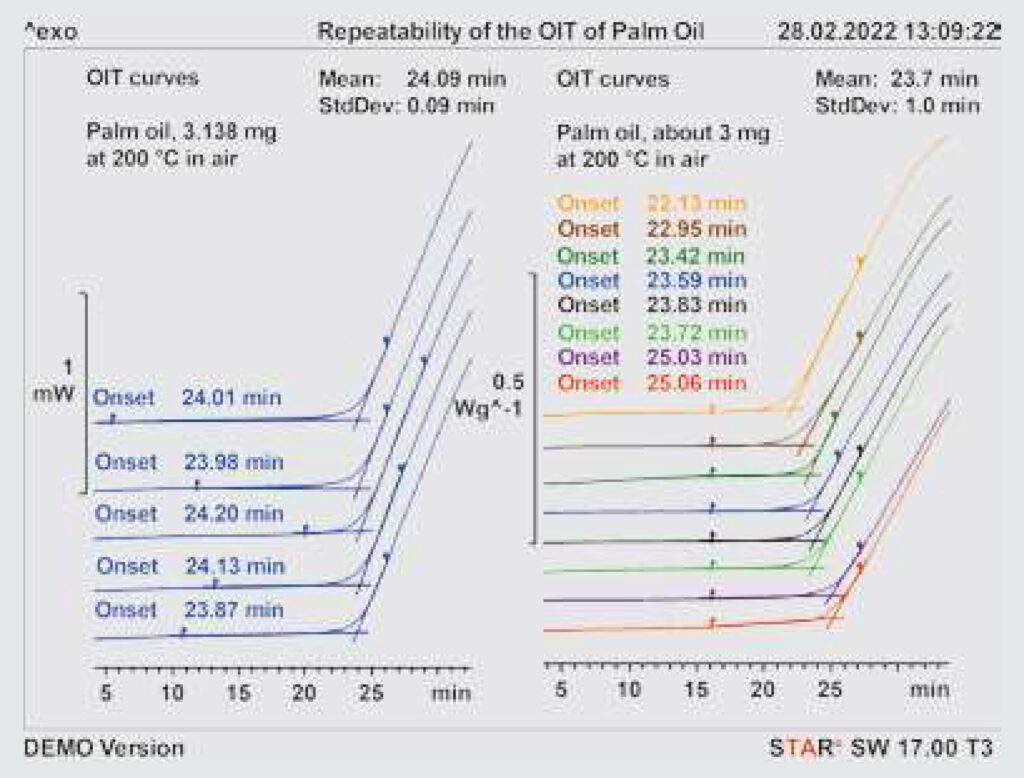
Rysunek 10. Zależność OIT od granic oceny (lewy wykres) i powtarzalności pomiarów OIT (prawy wykres). Szczegóły w tekście.
Komentarz: istnieją jednak oleje, które dają znacznie większe odchylenia standardowe przy zastosowaniu nieco innych wartości granicznych oceny. W tym względzie odchylenie standardowe wynoszące 0,09 min stanowi wartość optymalną. W przypadku innych olejów (np. oleju kokosowego), ten udział niepewności (w zależności od temperatury) może wynosić kilkadziesiąt sekund.
Znaczący wpływ na wyniki pomiarów OIT ma również przygotowanie próbki. Wykres po prawej stronie rysunku 10 przedstawia pomiary ośmiu próbek oleju palmowego (masa próbki około 3 mg) w temperaturze 200°C i ich ocenę. W wyniku oceny uzyskano średnią wartość OIT wynoszącą 23,7 min ± 1,0 min lub ± 5%. Wartość ta jest około trzy razy większa niż udział niepewności wynikający z niepewności temperatury w dobrze wyregulowanym DSC. Prowadzi to do wniosku, że zasadniczy wpływ na niepewność OIT w przypadku olejów ma przygotowanie próbki. Podczas przygotowywania próbki należy zatem zwrócić szczególną uwagę, aby olej znajdował się na środku podstawy tygla. Można to zrobić np. za pomocą strzykawki, przenosząc małą kroplę oleju na środek tygla. Dobrym rozwiązaniem będzie umieszczenie niewielkiej ilości oleju na dnie tygla. W każdym przypadku należy się upewnić, że cała próbka znajduje się na dnie tygla, a nie wokół jego krawędzi. Ponadto, w pomiarach porównawczych, stosowane masy próbek powinny być zawsze mniej więcej takie same: mierzony OIT wykazuje tendencję w zrostową dla prób ek o większej masie.
Oszacowanie temperatury do pomiarów OIT
Jak wspomniano wcześniej, optymalna temperatura dla pomiaru OIT jest często określana za pomocą pomiaru OOT. Na rysunku 11 przedstawiono zależności dla mierzonych tu olejów. Na osi x przedstawiono OOT pięciu olejów mierzone w powietrzu z ogrzewaniem 10 K/min, a na osi y różnic ę pomiędzy OOT a temperaturami izotermicznymi odpowiadającym i wybranym OIT (tutaj 10, 20, 30, 40, 50 i 60 min).
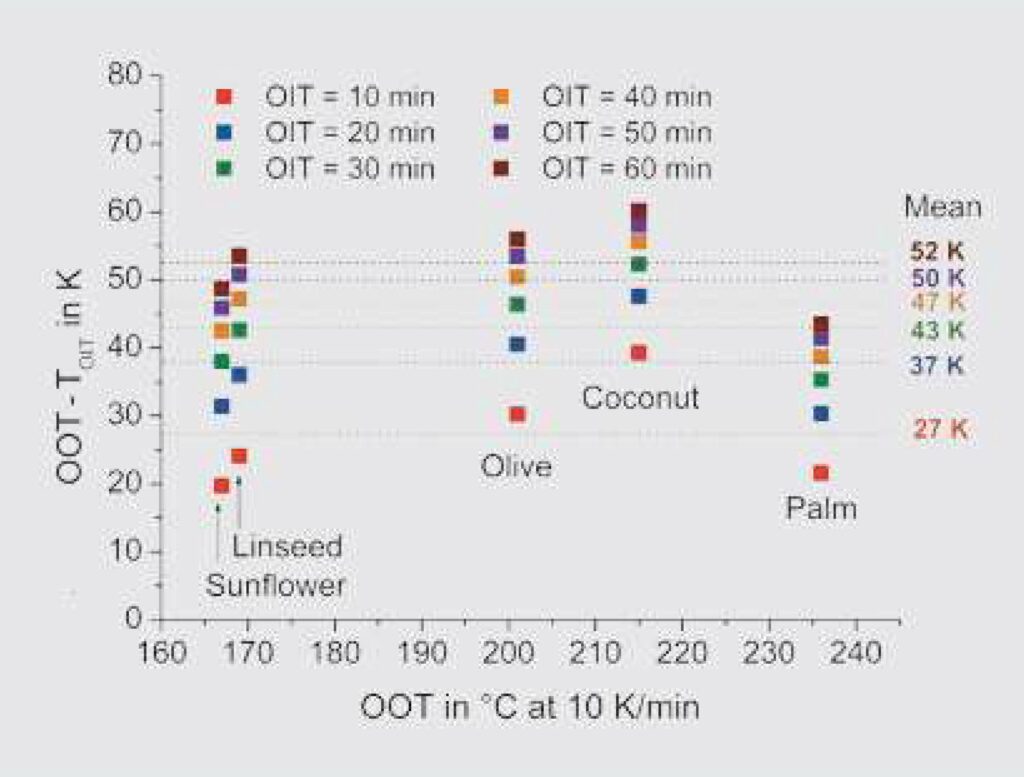
Rysunek 11. Zależność pomiędzy OOT – TOIT i OOT dla różnych OIT; pomiary w powietrzu; szybkość ogrzewania dla pomiarów OOT: 10 K/min; masa próbki około 3 mg.
Temperatury zostały obliczone przy pomocy wzoru 1. Zgodnie z oczekiwaniami, różnica ta wzrasta wraz ze wzrostem OIT. Jeśli te różnice zostaną uśrednione dla danego OIT dla różnych olejów, otrzymamy średnie war tości podane na r ysunku (również wykreślone jako linie przerywane).
Wykres wartości średnich w funkcji odpowiadających im OIT daje krzywą przedstawioną na rysunku 12. Można to opisać równaniem (krzywa ciągła):
OOT – TOIT = ΔTmax – ΔT0 ∙ e –OIT /τ
Tutaj ΔTma x jest różnicą temperatur pomiędzy OOT (mierzoną przy 10 K/min) a temperaturą, poniżej której nie można wyznaczyć OIT na krzywej DSC, ΔTmax – ΔT0 jest różnicą temperatur pomiędzy OOT (mierzoną przy 10 K/min) a temperaturą, w której mierzono OIT o długości 0 min, natomiast T jest stałą czasową. Ustalona tu zależność powinna stanowić użyteczną zasadę dla olejów służącą do szacowania odpowiedniej temperatury dla danego OIT. Przykład: olej mierzony przy 10 K/min w powietrzu ma temperaturę OOT równą 180°C. Chcemy wykonać pomiary OIT w powietrzu, które dają OIT około 25 minut. W jakiej temperaturze powinny być wykonywane pomiary OIT? Odpowiedź podano na rysunku 12 za pomocą niebieskich strzałek: odpowiednia temperatura OIT wynosi około (180 – 40)°C lub 140°C. Niepewność tego oszacowania wynosi ±6°C.
Komentarz: stwierdzenia zawarte w tym punkcie odnoszą się ilościowo t ylko do pomiarów OOT pr zy 10 K/min w powietrzu oraz pomiarów OIT w powietrzu. Inna szybkość grzania OOT lub użycie tlenu zamiast powietrza prowadzi do innych wyników.
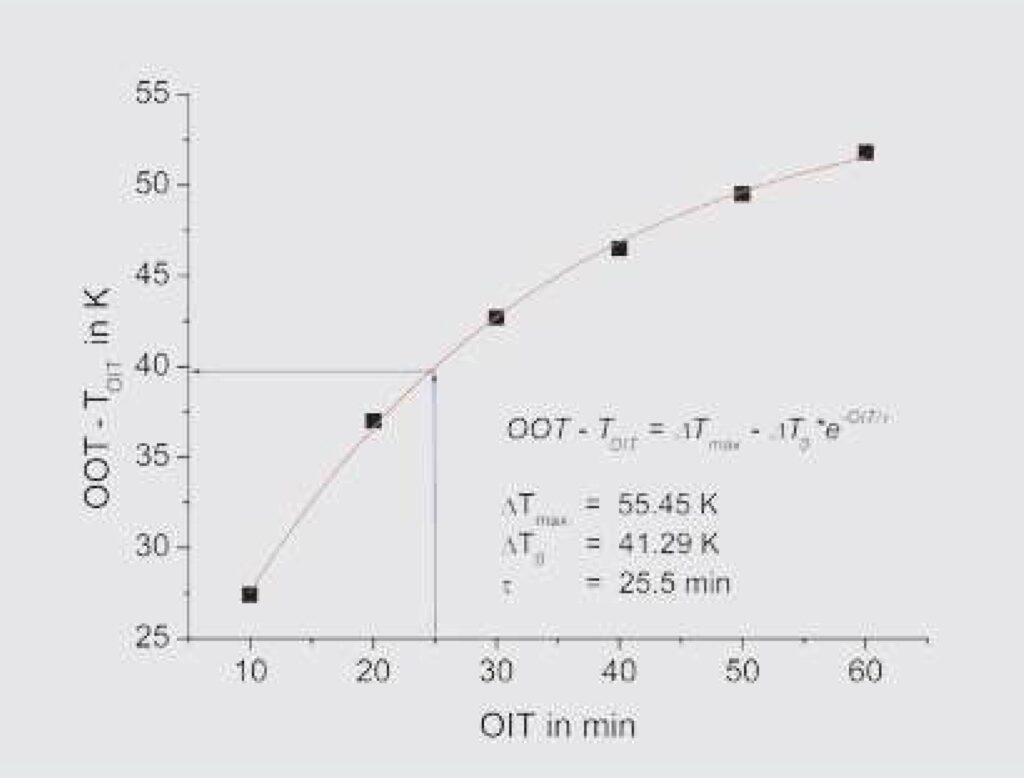
Rysunek 12. Zależność między OOT – TOIT i OIT mierzona w powietrzu; szybkość grzania dla pomiarów OOT: 10 K/min. Szczegóły w tekście.
Wnioski
Stabilność oksydacyjna olejów, tłuszczów i polimerów jest często charakteryzowana w warunkach izotermicznych przy pomocy tzw. czasu indukcji utleniania (OIT) dla danej temperatury. Wartości OIT mocno zależą od temperatury (T), w której są mierzone. W praktyce oznacza to, że kalibracja DSC powinna być również prowadzona przy użyciu niemal izotermicznych metod kalibracji. Dopiero wtedy możemy założyć, że zdefiniowana w metodzie pomiarowej temperatura izotermiczna jest rzeczywiście prawdziwa. Wpływ temperatury na niepewność OIT olejów wynosi około 7,3 ± 1,2%/K (ogólna zasada). Zależność OIT olejów (a także poliolefin) od temperatury można opisać funkcją Arrheniusa. Niepewność w określaniu OIT wynika głównie z niepewności temperatury izotermicznej, przygotowania próbki i oceny OIT (wybór stycznej). Największy udział w niepewności OIT olejów ma przygotowanie próbki. Z naszego doświadczenia wynika, że pomiar OIT powinien dawać OIT o długości 20 ± 5 minut. Czas ten stanowi dobry kompromis pomiędzy czasem trwania eksperymentu a niepewnością wyników. Komentarz końcowy: wiele wyników przedstawionych w tym artykule dotyczy olejów. Nie można tu udzielić odpowiedzi na pytanie, w jakim stopniu odnoszą się one do polimerów. Jednakże, metodologię przedstawioną w tym artykule można wykorzystać do oszacowania niepewności OIT dla wszystkich materiałów, które mogą być charakteryzowane za pomocą pomiarów OIT.
Literatura
[1] Teresa Dennenwaldt, Jessica Stromer, Isothermal calibration and adjustment, Part 2: Heating rate dependence of temperature measurement, UserCom 54, 1–5.
[2] Claus Franzke, Allgemeines Lehrbuch zur Lebensmittelchemie, ISBN 3-86022-234-1, 1996.

