Antybiotykooporność drobnoustrojów w kontekście aktualnego raportu WHO
Autor: Elżbieta Ograczyk, Sebastian Wawrocki, Adrian Gajewski, Malwina Kawka, Weronika Gonciarz, Karolina Rudnicka, Beata Sadowska, Magdalena Chmiela*
Coraz częściej występującą oporność drobnoustrojów na antybiotyki wiąże się z poważnymi zagrożeniami dla zdrowia publicznego. Skutkuje to wyczerpywaniem się opcji terapeutycznych, brakiem możliwości kontroli zakażeń, większym ryzykiem rozprzestrzeniania się drobnoustrojów, wydłużaniem czasu trwania infekcji, jak i hospitalizacji pacjentów, zwiększonymi kosztami, a w konsekwencji wyższą śmiertelnością.
Znaczenie tego problemu dostrzega Światowa Organizacja Zdrowia WHO (ang. World Health Organization), która wydała w 2014 roku dokument pt. „Oporność drobnoustrojów na antybiotyki: raport podsumowujący monitorowanie antybiotykoodporności na świecie w 2014 roku”. W tym opracowaniu podkreślono, jak ważnym problemem jest antybiotykooporność drobnoustrojów, która pomimo kolejnych odkryć naukowych i doskonalenia opcji terapeutycznych nadal stanowi poważny problem i zagrożenie w skali globalnej [21].
Ze względu na zaistniałą sytuację pojawia się pilna potrzeba kontroli zjawiska antybiotykoodporności. Jednakże, brak jest aktualnie obowiązujących wytycznych odnośnie gromadzenia danych w tym zakresie, stąd też są one fragmentaryczne i nie obejmują wystarczającej ilości informacji dotyczących zakażeń pozaszpitalnych. W odpowiedzi na ten problem WHO przygotowuje plan działania, obejmujący: opracowanie narzędzi i procedur monitorowania antybiotykooporności drobnoustrojów stanowiących zagrożenie dla ludzi, jak również zwierząt hodowlanych; śledzenie konsekwencji zdrowotnych i ekonomicznych zakażeń szczepami lekoopornymi; ustalenie form współpracy z ośrodkami zajmującymi się monitorowaniem antybiotykoodporności oraz wzmocnienie tego systemu na poziomie regionalnym, jak i globalnym [21].
Światowa Organizacja Zdrowia ogłasza również, iż ze względu na poważną sytuację w skali światowej w zakresie lekooporności drobnoustrojów pojawia się wysokie ryzyko nadejścia tzw. ery postantybiotykowej. Dochodzi również do dysproporcji pomiędzy tempem narastania tego zjawiska i wzrostem zapotrzebowania na nowe leki, a możliwościami pozyskania nowych środków przeciwbakteryjnych [21].
W raporcie WHO zwraca szczególną uwagę na lekooporność wirusa HIV (ang. Human Immunodeficiency Virus), wirusów grypy, prątków gruźlicy, a także pasożytów wywołujących malarię [21].
Wirus grypy
Grypa należy do chorób o charakterze sezonowym, związanych głównie z infekcjami układu oddechowego. Istnieją 3 typy wirusów: A, B i C powodujących takie infekcje. Najlepiej poznane są wirusy grupy A, które klasyfikowane są dodatkowo na podgrupy – w zależności od zmienności białek powierzchniowych, takich jak: neuranimidaza (N) oraz hemaglutynina (H), które determinują przyleganie wirusów do komórek nabłonka oddechowego gospodarza. Wirus grypy typu A występujący wśród ludzi został podzielony na podtypy: H1N1 i H3N2. W przypadku wirusów grypy typu B dokonano podziału na 2 linie: B/Yamagata oraz B/Victoria. Wirusy typu A i B występują w populacji ludzkiej stosunkowo często, wywołując zarówno epidemie, jak i pandemie, stąd też szczepy te stanowią podstawę do konstrukcji szczepionek przeciwko grypie sezonowej. Wirus typu C rozwija się znacznie rzadziej i zazwyczaj jest przyczyną infekcji o łagodnym przebiegu, co powoduje mniej znaczące konsekwencje dla zdrowia publicznego. Grypę charakteryzuje nagła gorączka, kaszel (zwykle suchy), ból głowy, bóle mięśni i stawów, złe samopoczucie, ból gardła i katar. U większości osób objawy ustępują w ciągu tygodnia bez konieczności korzystania z pomocy zakładów opieki medycznej. Jednakże grypa może mieć także przebieg ciężki i prowadzić do śmierci, szczególnie u osób z grup tzw. podwyższonego ryzyka, głównie u kobiet w ciąży, dzieci między 6 miesiącem a 5 rokiem życia, osób z obniżoną odpornością oraz u osób cierpiących na schorzenia przewlekłe [23].
Transmisja zakażenia i jej zapobieganie
Grypa rozprzestrzenia się łatwo i szybko, w szczególności w zatłoczonych miejscach, w tym w przedszkolach, szkołach, domach opieki czy środkach komunikacji miejskiej. Kiedy zarażona osoba kaszle lub kicha, kropelki zawierające wirusy zostają rozproszone w powietrzu i transmitowane są do osób znajdujących się w pobliżu. Ponadto wirus grypy może także przenosić się za pośrednictwem zanieczyszczonych rąk podczas bezpośredniego kontaktu z osobą zainfekowaną. Mając na uwadze taki sposób rozprzestrzeniania się wirusów grypy, w celach zapobiegawczych w sezonie grypowym zaleca się regularne mycie rąk oraz zakrywanie ust podczas kaszlu i kichania [23]. Najpowszechniejszą formą zapobiegania szerzeniu się zakażeń wywoływanych wirusem grypy są szczepienia sezonowe. Efektywne i bezpieczne szczepionki są dostępne na rynku od przeszło 60 lat. W środowisku osób zdrowych, szczepienia zapewniają ochronę przez rozwojem pełnoobjawowej grypy, nawet w przypadku gdy wirusy szczepionkowe nie odpowiadają ściśle typom wirusów znajdujących się w otoczeniu. Światowa Organizacja Zdrowia rekomenduje szczepienia dla kobiet w ciąży (w każdym stadium), dzieciom (5m-cy -5 lat), osobom starszym, powyżej 65 roku życia oraz pracownikom służby zdrowia. Przez wiele lat rekomendowana była szczepionka podjednostkowa – trójskładnikowa zawierająca 2 podjednostki wirusów typu A oraz 1 podjednostkę wirusa typu B. W 2014 roku wprowadzona została nowa szczepionka, 4-składnikowa z dodatkową podjednostką wirusa typu B. Ze względu na monitorowanie wirusów znajdujących się w środowisku i ich zmienność, co 2 lata skład szczepionek ulega zmianie [23, 24].
Leczenie
W niektórych krajach dostępne są leki przeciwwirusowe zapobiegające grypie, które zmniejszają poważne komplikacje oraz liczbę zgonów. Podanie leków zaleca się we wczesnych stadiach choroby, w ciągu pierwszych 48 godzin od wystąpienia objawów. Istnieją 2 klasy takich leków:
- Inhibitory białka neuraminidazy (np. oseltamiwir, zanamivir, peramivir czy laninamivir).
- M2 blokery kanału protonowego – adamantany (np. amantadyna czy rimantadyna).
WHO monitoruje wrażliwość na te leki krążących w środowisku wirusów grypy, aby zapewnić wczesne wskazówki dotyczące możliwości ich stosowania w leczeniu klinicznym i potencjalnej chemioterapii [8, 23, 24, 25].
Oporność wirusów grypy na leki przeciwwirusowe
Chociaż szczepionki nadal stanowią podstawowe narzędzie zapobiegania i kontroli grypy, w ciągu ostatnich 10 lat leki przeciwwirusowe były coraz częściej stosowane w leczeniu pandemii i epidemii tej choroby. WHO opublikowała wytyczne dotyczące ich stosowania w praktyce klinicznej [24]. Jak już wspomniano, obecnie dostępne są dwie klasy leków przeciwwirusowych do leczenia grypy: adamantany i inhibitory neuraminidazy. Jednak ze względu na szeroką oporność wirusów na adamantany, leki te nie są zalecane do stosowania w celu zwalczania wirusów grypy sezonowej i wirusów grypy typu B [1, 23]. Oporność na adamantany została wykryta w wirusach typu A (H3N2) po szybkim wzroście częstości ich występowania w latach 2004-2005. Wirusy grypy A (H1N1), które w 2009 roku wywołały pandemię, nabyły gen oporności na adamantany od rodzicielskiego wirusa świńskiej grypy pochodzącego z Eurazji. Inhibitory neuraminidazy: oseltamivir i zanamivir, opracowane w latach dziewięćdziesiątych, pozostają skuteczne przeciwko wirusom grypy typu A oraz B i są obecnie powszechnie dostępne [8].
Nadzór nad lekoopornością wirusów grypy
Odporność i zmniejszenie wrażliwości na leki przeciw grypie są wykrywane na podstawie testów laboratoryjnych izolatów wirusa pobranych od pacjentów z i bez narażenia na działanie leków przeciwwirusowych. Istnieją dwa zestawy laboratoryjnych metod wykrywania oporności lub jej spadku: testy genotypowe i testy fenotypowe. Metoda wykonywania testów wrażliwości wirusów na leki została opracowana przez GISRS (ang. Global Influenza Surveillance and Response System), głównie w krajach, w których stosowane są leki przeciwwirusowe. Chociaż wszystkie regiony WHO mają obecnie możliwość przeprowadzania tego typu testów, laboratoria korzystają z szerokiej gamy protokołów; dostępne są również standardy interpretowania i zgłaszania wyników testów. Testy wrażliwości wirusów są przeprowadzane przez Centra Współpracujące z GISRS WHO oraz niektóre krajowe ośrodki badawcze ds. grypy, dostarczając szerokich danych dotyczących podatności na grypę w trakcie każdego sezonu chorobowego [16, 23].
Uważa się, że Krajowe Centra ds. Grypy (ang. NIC – National Influenza Centers), są w stanie wygenerować bardziej aktualne dane dotyczące wrażliwości wirusów na chemioterapeutyki, niż jest to możliwe w dużych programach, które wymagają zebrania wyników badań i następnie ich globalnego opracowania, co jest rozciągnięte w czasie. Szybkość pozyskiwania wiarygodnych wyników ma kluczowe znaczenie dla wczesnego wykrywania opornych szczepów podczas leczenia. W 2011 r. utworzono ekspercką grupę roboczą WHO ds. Nadzoru nad nadwrażliwością na grypę, celem opracowania praktycznych podejść do kart charakterystyki GISRS, doradzającą w zakresie: odpowiedniej strategii nadzoru, metodologii laboratoryjnej, interpretacji danych z badań laboratoryjnych, kryteriów klasyfikacji wyników raportowania oraz jakości materiałów referencyjnych. Grupa ta kontroluje również wykorzystanie istniejących już leków przeciwwirusowych oraz stan prac nad rozwojem nowych chemioterapeutyków w badaniach klinicznych [23, 25].
Konsekwencje lekooporności wirusów grypy dla zdrowia publicznego
Stosowanie leków przeciwwirusowych w zwalczaniu wirusów grypy ma znaczenie dla zdrowia publicznego. Zapobiega zakażeniom u osób narażonych na duże ryzyko rozwoju ciężkiej choroby, zmniejsza zachorowalność i śmiertelności wśród takich osób, przyczynia się również do złagodzenia objawów infekcji oraz zmniejszenia transmisji wtórnej. W przypadku, gdy leki przeciwwirusowe zostają podane prawidłowo, dochodzi do zmniejszenia ryzyka zakażenia od 70% do 90% oraz skrócenia czasu trwania choroby do 1-2 dni. Dodatkowo dochodzi również do zmniejszenia komplikacji spowodowanych wtórnymi zakażeniami bakteryjnymi [24]. Jednakże nie zawsze wczesne wdrożenie terapii skutkuje sukcesem. Na przykład, wirusy grypy A (H5N1) o wysokim poziomie oporności na oseltamiwir zostały wykryte u dwóch wietnamskich pacjentów leczonych w styczniu 2005 r. [8]. Obaj chorzy zmarli, pomimo wczesnego rozpoczęcia leczenia (w ciągu 48 godzin od wystąpienia objawów) wysoką dawką leku [8]. Ponadto, oporność na leki przeciwwirusowe może komplikować podejście do leczenia klinicznego na kilka sposobów, łącznie z ograniczeniem możliwości zastosowania terapii skojarzonej.
Wirus HIV
Ludzki wirus niedoboru odporności HIV (ang. Human Immunodeficiency Virus) infekuje komórki układu odpornościowego, osłabiając ich funkcję lub powodując całkowite ich zniszczenie. Zakażenie nieleczone może prowadzić do postępującego wyniszczania układu odpornościowego i rozwoju zespołu nabytego braku odporności AIDS (ang. Acquired Immune Deficiency Syndrome). Według szacunków WHO i Wspólnego Programu Narodów Zjednoczonych Zwalczania HIV i AIDS – UNAIDS (ang. The Joint United Nations Programme on HIV and AIDS) pod koniec 2014 roku na świecie żyło 36,9 milionów osób zakażonych wirusem HIV. W tym samym roku około 2,5 miliona osób zostało zarażonych, a 1,7 miliona (w tym 230 tysięcy dzieci) zmarło z powodu AIDS [14, 21]. Stosowanie wczesnej diagnostyki i wprowadzenie projektów zapobiegających przenoszeniu wirusa wpłynęło na ograniczenie liczby nowych zakażeń. Wirus HIV jest główną przyczyną zachorowalności u osób w wieku 30-44 lat oraz piątą główną przyczyną chorób w innych grupach wiekowych. Stosowanie leków antyretrowirusowych spowodowało spadek umieralności u chorych na AIDS [14]. W regionie europejskim wirus HIV pozostaje jednym z najważniejszych problemów dla zdrowia publicznego bez wyraźnych oznak ogólnego spadku zakażeń. W tym obszarze w 2013 roku odnotowano około 30 tysięcy nowych zakażeń. Najwięcej z nich miało miejsce w Estonii, nieco mniej na Łotwie, w Belgii i Portugalii. W Europie najwięcej nowych zakażeń odnotowuje się w populacji mężczyzn utrzymujących kontakty seksualne z mężczyznami, natomiast w Polsce wśród osób heteroseksualnych [14, 26].
Patogeneza zakażenia
Głównym celem ataku wirusa HIV są aktywowane limfocyty T pomocnicze. Wirus wnika do ich wnętrza przyłączając się do powierzchniowych receptorów tych komórek, w tym receptora CD4 oraz receptorów dla chemokin: CCR5 lub CXCR4. HIV atakuje również inne typy komórek mające na swojej powierzchni cząsteczkę CD4, takie jak spoczynkowe limfocyty T pomocnicze, monocyty, makrofagi i komórki dendrytyczne. Wkrótce po zakażeniu wirusem HIV, swoiste limfocyty cytotoksyczne CD8+ zabijają komórki zainfekowane, a proces ten zachodzi przy udziale pomocniczych limfocytów T CD4+. Z czasem silna reakcja odpornościowa powoduje wyczerpanie się i utratę funkcji zarówno HIV swoistych limfocytów T jak i całej populacji limfocytów T [14]. Wirus charakteryzuje się dużą zmiennością genetyczną, co wpływa na spadek efektywności cytotoksycznej limfocytów naturalnie cytotoksycznych NK (ang. Natural Killer) oraz umożliwia unikanie kontroli układu odpornościowego gospodarza [19]. Cechą charakterystyczną występującą u osób zakażonych HIV jest stopniowe zmniejszenie się liczby limfocytów T CD4+ ze względu na zahamowanie ich proliferacji oraz niszczenie tych komórek spowodowane aktywacją układu odpornościowego.
Leczenie zakażeń HIV
W leczeniu zakażenia wirusem HIV stosuje się tzw. terapię przeciwretrowirusową, która w obecnej praktyce klinicznej obejmuje sześć klas leków przeciwretrowirusowych. Działają one zarówno przed połączeniem wirusa z komórką docelową (inhibitor fuzji łączący się z wirusową glikoproteiną 4 oraz inhibitory receptorów CCR5 zmieniające ich strukturę trzeciorzędową), uniemożliwiając wniknięcie wirusa do komórki, jak i wewnątrzkomórkowo na różnych etapach cyklu komórkowego (inhibitory odwrotnej transkryptazy, integrazy i proteazy). W terapii dostępne są również preparaty skojarzone, które zawierają trzy farmaceutyki będące kombinacją leków nukleozydowych i nienukleozydowych. Skojarzona trójlekowa terapia antyretrowirusowa została powiązana ze znaczącym zmniejszeniem szybkości rozwoju lekooporności oraz wyższym odsetkiem skutecznych terapii zarówno pod względem wirusologicznym oraz klinicznym (brak infekcji oportunistycznych i rozwoju nowotworów zależnych od wirusa HIV), jak i immunologicznym (wzrost liczby limfocytów T CD4+) [12, 15, 17].
Jednym z ważniejszych celów jakie niesie terapia antyretrowirusowa jest osiągnięcie pełnej skuteczności wirusologicznej, zapobiegającej pojawianiu się nowych mutacji determinujących lekooporność [5]. Oporność na leki antyretrowirusowe oraz jej zmienność stanowią zarówno przyczynę, jak i konsekwencję aktualnych problemów w terapii antyretrowirusowej i wiążą się z szeregiem czynników: aktywnością replikacyjną wirusa, siłą działania leku, barierą genetyczną, adherencją (zdolnością przylegania) wirusa czy zmiennością genetyczną gospodarza (Ryc. 1) [17].
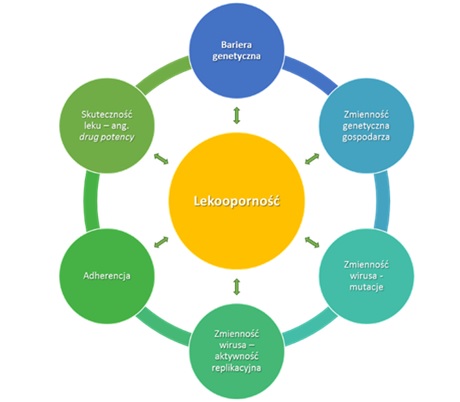
Ryc. 1. Czynniki wpływające na lekooporność wirusa HIV [17].
Lekooporność wirusa HIV
Rozwój lekooporności wirusów jest skutkiem ich dynamiki replikacyjnej pod działaniem presji selekcyjnej leku. Każdy cykl replikacyjny pozwala na zwiększenie zmienności genetycznej wirusa, (jedna do dwóch mutacji na jedną replikację genomu HIV-1). Należy podkreślić, że większość nowych zmutowanych populacji to wirusy defektywne. Ze względu na częste pojawianie się błędów wprowadzanych przez odwrotną transktyptazę HIV, mutacje powstają spontanicznie. Początkowo występuje zjawisko tzw. niskiej aktywności replikacyjnej (ang. viral fitness), następnie pojawiają się mutacje wtórne, poprawiające efektywność namnażania wirusa [13, 17].
Skutkiem rozwoju oporności na leki antyretrowirusowe może być również ryzyko oporności krzyżowej na kilka farmaceutyków z jednej grupy terapeutycznej (leków o podobnym mechanizmie działania) i zwiększenie ryzyka szerzenia się zakażenia HIV. Konieczna jest w takim przypadku zmiana leczenia na terapię opartą na schemacie bardziej złożonym oraz wymagającym częstszego dawkowania. Jednakże taka terapia będzie obarczona nasileniem działań niepożądanych i zwiększeniem kosztów leczenia. Lekooporność przekłada się również na skrócenie okresu skuteczności kolejnego schematu terapeutycznego oraz zwiększenie ryzyka akumulacji kolejnych mutacji i transmisji wariantów opornych. Istnieje również pozytywny aspekt pojawiania się mutacji związanych z lekoopornością, polegający na często obserwowanym zmniejszeniu aktywności replikacyjnej wirusów zmutowanych w porównaniu z wirusem o typie dzikim, o pełnej lub częściowej wrażliwości.
Rosnąca w szybkim tempie lekooporność wirusa HIV skłania lekarzy do stosowania nowych schematów leczenia opierających się na kluczowych kryteriach tj. :
- łatwość dawkowania,
- ocena ryzyka toksyczności,
- wystąpienie interakcji między stosowanymi lekami,
- możliwe inne opcje terapeutyczne
Zwykle konieczne jest zastosowanie dwóch lub trzech aktywnych leków w nowym zestawie (włączając aktywne leki z klas uprzednio używanych) [6, 17]. W każdym schemacie terapeutycznym powinien znaleźć się co najmniej jeden w pełni aktywny inhibitor proteazy oraz lek z klasy dotychczas nie używanej (np. inhibitor CCR5 – po uzyskaniu wyniku badania tropizmu, inhibitor fuzji lub integrazy) [6, 12].
Terapia genowa w leczeniu zakażeń HIV
Opisana wcześniej terapia antyretrowirusowa może znacznie zmniejszyć miano wirusa w osoczu. Jest ona jednak kosztowna i nie prowadzi do całkowitego wyleczenia. Naprzeciw wychodzi terapia genowa, która stanowi alternatywę leczenia antyretrowirusowego, ponieważ może prowadzić do opanowania zakażenia już po jednym zabiegu. Terapia genowa polega na pobraniu krwiotwórczych komórek macierzystych od pacjenta, wprowadzeniu genu terapeutycznego i po leczeniu ablacyjnym przeszczepieniu komórek z transdukowanym genem. Wprowadzane geny są tak zaprojektowane, aby ich produkt kolidował z kluczowymi etapami replikacji wirusa: poprzez bezpośredni wpływ na wiriony lub poprzez wpływ na czynniki komórkowe niezbędne do cyklu życiowego HIV. Po pilotażowych badaniach klinicznych nadal prowadzone są prace nad poprawą skuteczności wprowadzania genu oraz nad osiągnięciem długoterminowego efektu terapeutycznego [9].
Zakażenia wirusem HIV to stały problem całego świata, z którym walkę toczy się od lat. Pomimo dostępności wielu opracowań naukowych dotyczących patogenezy wirusa oraz złożonych reakcji odpornościowych w przebiegu choroby, nie udało się opracować skutecznego leczenia antyretrowirusowego. Nadzieją dla zakażonych pacjentów stają się trwające prace nad poprawą skuteczności i bezpieczeństwa terapii genowej oraz wynalezieniem szczepionki mogącej zapobiegać nowym zakażeniom.
Gruźlica
Czynnikiem etiologicznym rozwoju gruźlicy (TB) u ludzi są prątki Mycobacterium tuberculosis (M. tuberculosis) należące do grupy Mycobacterium tuberculosis complex, w skład, której wchodzą również M. bovis, M. bovis BCG, M. africanum i M. microti. Rola M. tuberculosis w rozwoju gruźlicy została opisana po raz pierwszy już w roku 1882 przez niemieckiego uczonego Roberta Kocha. Drobnoustroje wyizolowane przez badacza ze zmian chorobowych charakteryzowały się pałeczkowatym lekko zagiętym kształtem, długością do 10 μm i szerokością około 0,4 μm, jak również brakiem zdolności ruchu i wytwarzania przetrwalników. Dalsze badania prowadzone przez liczne grupy badaczy wykazały inne cechy wyróżniające prątki z grupy organizmów prokariotycznych. Najbardziej charakterystyczną cechą tych bakterii jest ich ściana komórkowa zawierająca znaczne ilości lipidów, takich jak kwasy mykolowe składające się z długich łańcuchów zawierających 60-90 atomów węgla, glikolipidy i woski. Obecność w ścianie prątków licznych związków o charakterze lipidowym determinuje oporność tych mikroorganizmów na detergenty, a także na wysychanie. Wiele tych komponentów stanowi ważne czynniki chorobotwórczości prątków [4, 7, 11, 20].
Dane statystyczne wskazują jednoznacznie, iż obecnie gruźlica pozostaje nadal jedną z najbardziej śmiertelnych chorób zakaźnych. W roku 2015 chorobę tę zdiagnozowano u ponad 10,4 miliona osób na świecie, natomiast aż 1,4 miliona chorych zmarło z jej powodu, w tym przeszło 400 tys. osób cierpiących na współistniejące zakażenie wirusem HIV [27].
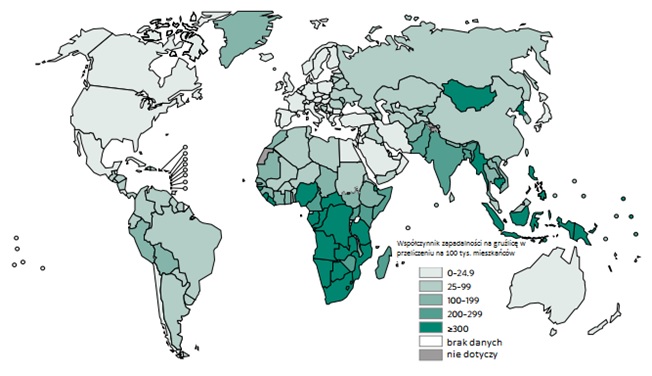
Ryc. 2. Zapadalność na gruźlicę w przeliczeniu na 100 tysięcy mieszkańców.
Diagnostyka gruźlicy umożliwiająca wczesne wykrycie choroby jest mało efektywna. Gruźlica stanowi również narastający problem w kontekście wzrastającej liczby przypadków występowania szczepów lekoopornych i wielolekoopornych – MDR (ang. multi-drug resistant). W samym 2015 roku zanotowano 580 tys. nowych przypadków gruźlicy MDR. Nabieranie oporności na farmaceutyki przez prątki gruźlicy rozpoczęło się krótko po wprowadzeniu do użycia pierwszych leków. Randomizowane badania kliniczne z lat 40. XX wieku wykazały, iż drobnoustroje szybko nabywają mechanizmów odporności. Dlatego też obecnie terapia przeciwgruźlicza bazuje na wykorzystaniu kombinacji 4 leków: ryfampicyny, izoniazydu, etambutolu i pirazynamidu podczas długotrwałej, bo co najmniej 6 miesięcznej kuracji. Jednak szczególnej uwagi wymagają przypadki zakażeń szczepami MDR, gdzie proces leczenia trwać może nawet dwa lata i wymagać codziennego podawania mieszanki leków cechujących się niejednokrotnie efektami ubocznymi [2, 27].Pierwsze kompleksowe badania skupiające uwagę na gruźlicy opornej na leki pochodzą z roku 2006 i przeprowadzone zostały przy współpracy Centrum Zapobiegania i Kontroli Chorób – CDC (ang. Centres for Disease Control) i WHO, badania te wykazały, iż przeszło 20% izolowanych szczepów M. tuberculosis cechuje oporność na wybrane leki pierwszego wyboru wspomniane powyżej. Co więcej raport ukazał problem, jakim stają się obecnie szczepy MDR oraz XDR (ang. extensively drug resistant) oporne także na leki drugiego rzutu takie jak amikacyna, kapreomycyna i pochodne fluorochinolonów. Szczepy te zostały zidentyfikowane w każdym z 25 światowych laboratoriów referencyjnych. Niebezpieczną sytuację ekspansji szczepów lekoopornych pogłębia również fakt, iż spośród 580 tys. przypadków zdiagnozowanych w roku 2015, terapię wdrożono jedynie u 20% osób [11, 27].
MDR-TB jest wywoływana przez bakterie, które nie reagują na dwa najsilniejsze leki pierwszego rzutu przeciwko gruźlicy: izoniazyd i ryfampicynę. Jednakże, MDR-TB można wyleczyć stosując leki drugorzędowe, choć są one generalnie mniej skuteczne, droższe i zwykle bardziej toksyczne w porównaniu do leków pierwszego rzutu. Natomiast bakterie, które powodują XDR-TB, nie reagują nawet na najsilniejsze drugorzędowe leki przeciwprątkowe. W rezultacie, osoby z gruźlicą oporną na leki poddawane są terapii, która zazwyczaj obejmuje kombinację chemioterapeutyków i bardzo silnych leków przeciwprątkowych podawanych w formie cykli intensywnych okresów leczenia i przerw w celu regeneracji organizmu. Typowy okres leczenia MDR-TB wynosi 20-26 miesięcy, a leczenie XDR-TB trwa nawet ponad 32 miesiące. Stanowi to duże obciążenie dla osób leczonych i powodować może poważne skutki uboczne obejmujące depresję, psychozę, upośledzenie słuchu, zapalenie wątroby, upośledzenie czynności nerek, utratę zdolności ruchowych, upośledzenie wzroku czy napady padaczkowe [2, 27].
Pomimo trudnej sytuacji, obiecujące są efekty bieżących wysiłków na rzecz wyeliminowania gruźlicy. Od 1990 r. wskaźnik śmiertelności gruźlicy zmniejszył się o przeszło 47%. Dodatkowo nieznacznie zwiększona została skuteczność diagnostyki i leczenia gruźlicy, co pozwoliło od 2000 r. ocalić ponad 49 milionów osób. Aktualne badania nad gruźlicą lekooporną wykazują duży potencjał dotyczący skrócenia czasu leczenia i minimalizowania skutków ubocznych dla pacjentów [2, 27].
Mimo ogólnoświatowych wysiłków i dążeń na rzecz wyeliminowania choroby, jaką jest gruźlica, a także wyznaczenia przez WHO, roku 2035 jako tego w którym ma nastąpić redukcja o co najmniej 90% liczby zgonów powodowanych przez gruźlicę i częstości zachorowań, wiele programów zapobiegawczych nadal zaniedbuje kwestię lekooporności. Dodatkowo, wysiłki na rzecz eliminacji gruźlicy są jeszcze bardziej skomplikowane przez niedawne pojawienie się szczepu M. tuberculosis całkowicie opornego na działanie znanych leków, a także obecne współzależności gruźlicy i HIV / AIDS w krajach afrykańskich. Najistotniejszymi elementami w walce z gruźlicą oporną na leki, musi, więc stać się rozszerzenie profilaktyki gruźlicy lekowrażliwej, zdobywanie bardziej kompleksowych danych na temat nowych przypadków w skali globalnej, wzrost nakładów finansowych na leczenie gruźlicy i badania kliniczne nad nowymi lekami [27].
Malaria
Malaria (zimnica) to tropikalna choroba pasożytnicza, której czynnikiem etiologicznym są pierwotniaki z rodzaju Plasmodium. Spośród pięciu gatunków (P. falciparum, P. vivax, P. ovale, P. malariae, P. knowlesi) wywołujących malarię u ludzi, P. falciparum oraz P. vivax odpowiedzialne są za najwięcej przypadków zarażeń. Zimnica występuje w wielu krajach strefy tropikalnej i subtropikalnej, a narażonych na zachorowanie jest około 1 miliarda osób. Według danych WHO w 2010 roku odnotowano aż 219 milionów przypadków malarii na świecie, zaś 660 tysięcy osób zmarło z powodu tej choroby [21]. W Polsce rocznie leczy się od 10 do 30 przypadków inwazji Plasmodium, które dotyczą głównie osób wracających z krajów endemicznych [22].
Patogeneza zarażenia
Do zarażenia dochodzi poprzez ukąszenie samicy komara z rodzaju Anophelesi i wprowadzenie sporozoitów (forma inwazyjna pierwotniaka) do krwioobiegu gospodarza wraz ze śliną komarzycy. Po przedostaniu się do wątroby, sporozoity namnażają się w hepatocytach (komórki wątroby) by po przekształceniu i pęknięciu uwolnić do krwi merozoity atakujące krwinki czerwone (erytrocyty). To właśnie rozpad erytrocytów odpowiedzialny jest za wystąpienie charakterystycznych objawów zarażenia typowych dla malarii takich jak wysoka temperatura, anemia, hemoglobinuria, hipoglikemia czy obniżenie ciśnienia krwi spowodowane zapaścią krążeniową [3]. Z uwagi na fakt, iż malaria w bardzo krótkim czasie może stać się chorobą zagrażającą życiu, czego powodem jest długotrwałe niedotlenienie organów wewnętrznych, podstawą programów zwalczania malarii jest szybkie i efektywne leczenie. Większość preparatów używanych w leczeniu zimnicy oparta jest na eliminacji form pasożyta znajdujących się we krwi, i są to chlorochina, atowakwon z prokwanilem (Malarone®), artemeter z lumefantryną (Coartem®), meflochina (Lariam®), sulfadoksyna z pirymetaminą (Fansidar®), czy też chinina skojarzona z antybiotykami takimi jak doksycyklina lub klindamycyna. Dobór leczenia oparty jest głównie na gatunku Plasmodium jakim zarażony jest pacjent, jego statusie klinicznym oraz wrażliwości zarodźca na leki przeciwmalaryczne.
Lekooporność
Zasadniczym problemem leczenia malarii jest rosnąca lekooporność zarodźców na stosowane leki. Według WHO oporność na leki przeciwmalaryczne definiowana jest jako zdolność pasożyta do przeżycia i namnażania się pomimo stosowania chemioterapeutyku w dawce zalecanej bądź też wyższej, lecz nadal tolerowanej przez pacjenta. Nabywanie lekooporności przez zarodźce malarii opiera się na powstawaniu spontanicznych mutacji w obrębie genomu. W przypadku niektórych leków wystarczy zaledwie jedna mutacja punktowa podczas gdy dla innych konieczne jest zajście mutacji wielokrotnych. Jeśli zaistniałe zmiany genetyczne nie wpłyną na zdolność zarodźca do rozmnażania się i przeżycia, pasożyty podatne na stosowany lek zostaną wyeliminowane, zaś oporne przeżyją utrwalając tym samym oporność na dany terapeutyk w całej populacji. Oporność P. falciparum na stosowaną kiedyś rutynowo chlorochinę stwierdzono po raz pierwszy pod koniec lat 50. XX wieku na terenie południowo-wschodniej Azji, zaś z biegiem lat rozprzestrzeniała się ona w innych krajach Azji, Afryki oraz Ameryki Południowej. P. falciparum nabył również oporność na prawie wszystkie obecnie dostępne leki przeciwmalaryczne, lecz jest ona mniej rozprzestrzeniona geograficznie [22].
Podczas trawienia hemoglobiny przez zarodźca powstają toksyczne produkty uboczne, które redukowane są do nietoksycznej hemozoiny. Uważa się, iż oporność P. falciparum związana jest z mutacją w genie Pfcrt kodującym białko z rodziny transporterów, odpowiedzialne za transport leków i metabolitów przez błonę komórkową. Skutkiem mutacji jest zwiększona zdolność pasożyta do wydalania chlorochiny, przez co niemożliwe staje się osiągnięcie stężenia terapeutycznego tego leku, potrzebnego do zahamowania hydrolizy hemoglobiny [10]. W przypadku P. vivax, którego oporność na chlorochinę opisano po raz pierwszy w 1989 roku na terenie Papui-Nowej Gwinei, dochodzi do mutacji w obrębie dwóch genów: Pvmdr1, który jest genem oporności oraz Pvcrt-o, który koduje białko transporterowe, lecz mechanizm lekooporności nadal pozostaje nieznany [18]. Celem większości programów zwalczania malarii jest ograniczenie liczby przypadków i zgonów związanych z zimnicą, co sprawiłoby, iż choroba ta przestałaby być poważnym problemem zdrowia publicznego.
Skuteczność terapeutyczną leków przeciwmalarycznych można ocenić jedynie poprzez oszacowanie efektywności terapii. W tym celu WHO opracowało wystandaryzowany protokół TES (ang. therapeutic efficacy study) umożliwiający uzyskanie wysokiej powtarzalności wyników, w którym zawarte są wytyczne dotyczące wykonywania badań klinicznych i parazytologicznych po 24 i 48 dniach nadzorowanego leczenia pacjenta. Prowadzone w kraju endemicznym badania według protokołu TES, stanowią podstawowe źródło danych umożliwiających monitorowanie zmian we wrażliwości zarodźców na leki przeciwmalaryczne jak i stanowiących podstawę wprowadzania terminowych zmian w stosowanych schematach leczenia [18].
Podsumowanie
Niniejszy artykuł ma na celu pokazanie, iż oporność drobnoustrojów na antybiotyki należy do bardzo poważnych problemów obejmujących swoim zasięgiem cały świat. WHO ostrzega, że w przyszłości ludzie znów mogą umierać z powodu chorób, które jeszcze dziś stanowią niewielkie zagrożenie dla zdrowia, a które leczyło się przez ostatnie lata antybiotykami. Chodzi zwłaszcza o choroby zakaźne. Konsekwencje rozprzestrzeniania się drobnoustrojów lekoopornych, zaniedbywania szczepień ochronnych i stale pogarszającego się zdrowia publicznego mogą być w przyszłości katastrofalne. Czas powrócić do starej jak świat maksymy, że lepiej zapobiegać niż leczyć, dbając o odporność oraz zdrowie swoje i innych. Tymczasem, zaleca się przede wszystkim szczepienia ochronne oraz dbałość o odpowiednie leczenie, w tym przyjmowanie antybiotyków tylko w uzasadnionych przypadkach.
Literatura
- Bright R.A., Medina M.J., Xu X., Perez-Oronoz G., Wallis T.R., Davis X.M. et al. „Incidence of adamantane resistance among influenza A (H3N2) viruses isolated worldwide from 1994 to 2005: a cause for concern.” Lancet, 2005, 366(9492):1175-1181. (http://www.ncbi.nlm.nih.gov/pubmed/16198766, accessed 8 April 2014).
- CDC. Treatment Regimens for Latent TB Infection (LTBI), 2016, Retrieved March 6, 2017, from Centers for Disease Control and Prevention, https://www.cdc.gov/tb/topic/treatment/ltbi.htm
- CDC, https://www.cdc.gov/malaria/
- Daniel T.M., Bates J.H., Downes K.A., “History of Tuberculosis. Tuberculosis”, 2006, 100(11), 1862-1870. doi:10.1128/9781555818357.ch2
- De Luca A., “The impact of resistance on viral fitness and its clinical implications. In: Geretti AM (ed.). Antiretroviral Resistance in Clinical Practice.”, 2006, Mediscript, London.
- European AIDS Clinical Society. Guidelines. Version 6.1 – November 2012. European AIDS Clinical Society (online) 2012; http://www.eacsociety.org/ Portals/0/files/pdf%20files/EacsGuidelines-v6.1–2edition.pdf
- Grzelewska-Rymanowska, I. „Gruźlica płuc.” 2003.Wydawnictwo Sesja, Łódź
- Gupta R.K., Nguyen-Van-Tam J.S. „Oseltamivir resistance in influenza A (H5N1) infection.” 2006,N Engl J Med, 354(13):1423-1424, author reply 1423-1424. (http://www.ncbi.nlm.nih.gov/pubmed/16571890, accessed 8 April 2014).
- Herrera-Carrillo E., Berkhout B. “Bone marrow gene therapy for HIV/AIDS Viruses”, 2015; 7(7): 3910-3936.
- Hiasindh Ashmi A. oraz Subhash Chandra P., “Antimalarial drug resistance: An overview.”, 2016, Trop Parasitol 6(1): 30-41,
- “History of Tuberculosis.” (2015). Retrieved March 6, 2017, Rutgers Global Tuberculosis Institute, http://web.njms.rutgers.edu/ntbcweb/abouttb/historyoftb.html
- Horban A., Podlasin R., Cholewińska G. et al. “Zasady opieki nad osobami zakażonymi HIV. Zalecenia PTN AIDS.”, 2013. Agencja Wydawnicza EkoPress, Warszawa.
- Johnson VA, Brun-Vezinet F, Clotet B et al., “Update of the drug resistance mutations in HIV-1.” December 2009. Top HIV Med 2009;17(5):138–145.
- Maartens G., Celum C. Lewin SR. HIV infection: epidemiology, pathogenesis, treatment and prevention. Lancet 2014; 19;384: 258-71
- Nachega J.B., Marconi VC, van Zyl G.U. et al., “HIV treatment adherence, drug resistance, virologic failure: evolving concepts.”, 2011, InfectDisordDrugTargets; 11(2):167–174.
16.Neumann G., Noda T, Kawaoka Y., “ Emergence and pandemic potential of swine-origin H1N1 influenza virus.”,2009,Nature, 459(7249):931-939. doi:10.1038/nature08157.
- Parczewski M., „Lekooporność u osób z zakażeniem HIV-1.”, 2013, Forum Zakażeń 2013;4(5):317–323.
- Rungsihirunrat K,, Muhamad P, Chaijaroenkul W, Kuesap J, Na-Bangchang K., “Plasmodium vivax drug resistance genes; Pvmdr1 and Pvcrt-o polymorphisms in relation to chloroquine sensitivity from a malaria endemic area of Thailand.”, 2015 Korean J Parasitol 53(1): 43-9.
- Smith S.A., Derdeyn C.A., “Harnessing the protective potential of HIV-1 neutralizing antibodies.”F1000Res 2016; https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4754033/
- Szewczyk, R., Kowalski, K., Janiszewska-Drobińska, B., Druszczyńska, M., “Rapid method for Mycobacterium tuberculosis identification using electrospray ionization tandem mass spectrometry analysis of mycolic acids. Diagnostic Microbiology and Infectious Disease.”, 2013, 76: 298-305.
- WHO, “Antimicrobial Resistance Global Report on Surveillance, 2014.”, World Health Organizations, URL
- WHO, “Drug resistance in malaria.”, 2001 URL
- WHO, “Fact sheet N°211, Influenza. Geneva.”, 2003. (http://www.who.int/mediacentre/ factsheets/2003/fs211/en/, accessed 9 December 2013).
- WHO, “WHO guidelines for pharmacological management of pandemic influenza A(H1N1) 2009 and other influenza viruses. Geneva, World Health Organization.” 2010.(http://www.who.int/csr/resources/publications/ swineflu/h1n1_guidelines_pharmaceutical_mngt.pdf?ua=1, accessed 13 February 2014)
- WHO, “Influenza A(H1N1) virus resistance to oseltamivir. Geneva, World Health Organization.” 2008.
(http://www.who.int/influenza/patient_care/antivirals/oseltamivir_summary…, accessed 9 December 2013). 32. Laboratory methodologies for testing the antiviral susceptibility of influenza viruses. Geneva, World Health Organization, 2012. (http://www.who.int/influenza/gisrs_laboratory/antiviral_susceptibility/en/, accessed 9 December 2013).
- WHO, „Sytuacja epidemiologiczna w HIV/ AIDS w Europie – 2013. Na podstawie raportu HIV/AIDS surveillance in Europe 2013. ECDC, WHO.”, 2014. Europejskie Centrum ds. Zapobiegania i Kontroli Chorób (ECDC), Sztokholm. http://www.aids.gov.pl/wspolpraca_miedzynarodowa/720/
- WHO. “What is TB? How is it treated?”, 2016Retrieved March 6, 2017, from World Health Organization, http://www.who.int/features/qa/08/en/
*Katedra Immunologii i Biologii Infekcyjnej, Wydział Biologii i Ochrony Środowiska, Uniwersytet Łódzki
