Niekonwencjonalne metody przygotowania próbek wodnych do oznaczeń chromatograficznych
Autor: Jacek Staniewski
Przygotowanie próbki przed końcowym oznaczaniem metodą chromatografii gazowej lub cieczowej stanowi niezwykle istotny etap procedury analitycznej. Ocenia się [1,2], że przygotowanie próbki zajmuje co najmniej połowę czasu realizacji całej procedury. Może być również jednym z głównych źródeł błędów. Problematyce przygotowania próbek ze względu na wagę problemu poświęcony jest cykliczny dział przeglądowy Modern Extraction Techniques w czasopiśmie Analytical Chemistry [3,4].
Skrócenie czasu przygotowania próbki i prostota metodyki, zwiększenie selektywności wydzielania analitów, poprawa własności analitycznych oznaczeń (dokładność i precyzja, granica wykrywalności i oznaczalności) [5] to główne cechy jakie powinien spełniać etap przygotowania próbki. Niezwykle istotne są również wymagania „zielonej” chemii analitycznej [6,7] głównie w zakresie wyeliminowania lub zmniejszenia zużycia rozpuszczalników. Miniaturyzacja procesu, szczególnie w połączeniu z jego automatyzacją lub robotyzacją i bezpośrednim połączeniem z końcowym oznaczaniem metodą chromatografii gazowej lub cieczowej dopełniają wymaganych cech współczesnych metod analitycznych. W rzeczywistości nie można wskazać metody posiadającej wszystkie pożądane cechy współczesnych metod analitycznych, tak samo jak nie można wskazać najlepszej metody do oznaczeń określonej grupy związków – wybór metody będzie nie tylko kompromisem pomiędzy oczekiwanymi zaletami a akceptowalnymi wadami, ale będzie także związany z celem oznaczeń i ich ilością oraz możliwościami analitycznymi laboratorium. W praktyce najczęściej stosowane są takie metody takie jak: – ekstrakcja do fazy stałej (SPE – Solid-Phase Extraction) – główną zaletą tej metody jest małe zużycie rozpuszczalników, selektywność procesu wydzielania oraz możliwość oczyszczenia próbki, – mikroekstrakcja do fazy stacjonarnej (SPME – Solid-Phase MicroExtraction) – bezrozpuszczalnikowa metoda oparta na podziale pomiędzy fazę stacjonarną umieszczoną na włóknie a próbkę wodną lub pomiędzy fazę na włóknie a warstwę nadpowierzchniową próbki wodnej, bardzo łatwo automatyzowana, – ekstrakcja ciecz-ciecz – pomimo zużycia znacznych ilości rozpuszczalników powszechnie stosowana w wielu laboratoriach ze względu na prostotę, a także prawie całkowite wydzielenia przy kilkukrotnej ekstrakcji. Metody te można określić mianem metod konwencjonalnych. Posiadają one, za wyjątkiem ekstrakcji ciecz-ciecz, bardzo silne wsparcie handlowe i techniczne. Do tej grupy zaliczyć można również ekstrakcję do fazy stacjonarnej na pręcie mieszającym (SBSE – Stir Bar Sorptive Extraction) [8]. Drugą grupę stanowić będą metody przygotowania próbek, które określić można jako metody niekonwencjonalne – obejmują one nowe metody przygotowania próbek ciekłych do oznaczeń chromatograficznych lub procedury będące daleko idącą modyfikacją metod konwencjonalnych. Wymienić tutaj można między innymi: – mikroekstrakcja ciecz-ciecz – realizowana w postaci różnych wariantów, wspólną ich cechą jest małe zużycie rozpuszczalnika wynoszące od kilkunastu mikrolitrów do kilku mililitrów. – ekstrakcja cieczą w obecności przegrody membranowej – grupa ta obejmuje zarówno typowe metody membranowe jak i metody ekstrakcyjne z nieporowatą membraną. – ekstrakcja (sorpcja) do fazy stacjonarnej lub warstwy adsorpcyjnej umieszczonej w kapilarze. Mikroekstrakcja ciecz-ciecz niezależnie o wariantu jest prostą metodą wydzielania wykorzystująca podział pomiędzy dwie fazy. W grupie tej znajdują się procedury znane w literaturze anglojęzycznej jako SDME Single Drop Microextraction [9], LPME Liquid-Phase Microextraction [10,11], LLME Liquid-Liquid Microextraction [12-16] oraz proponowana ostatnio bardzo szybka procedura ekstrakcyjna DLLME Dispersive Liquid-Liquid Microextraction [17-19]. Efektywność wydzielenia związku w mikroekstrakcji ciecz-ciecz zależy zarówno od jego własności fizykochemicznych jak i własności zastosowanego rozpuszczalnika.
W tabeli 1 przedstawiono przykładowe wyniki ekstrakcji fenoli z wody różnymi rozpuszczalnikami [15,16]. Fenole były ekstrahowane w formie wolnej ze środowiska kwaśnego lub po ich uprzedniej bezpośredniej derywatyzacji w wodzie do pochodnych acetylowych. Wydzielenie nie derywatyzowanych fenoli zachodzi ze stosunkowo niską efektywnością. Po derywatyzacji fenoli do mniej polarnej formy efektywność wydzielenia znacznie wzrasta. Ekstrakcja toluenem lub węglanem dietylu pozwala uzyskać wydzielenie z efektywnością znacznie przekraczającą 80%. Wysokie wydzielenie do węglanu dietylu związane jest z oddziaływaniami pomiędzy cząsteczkami rozpuszczalnika a cząsteczkami fenoli. Zwiększenie wydzielanie związków uzyskać można również przez wysolenia próbki, przy czym najczęściej stosowany jest w tym celu chlorek sodu. Wysolenie próbki ma szczególnie istotne znaczenie przy większym stosunku fazy wodnej do fazy organicznej [15,16]. Przy wysoleniu próbki należy jednak wziąć pod uwagę możliwość tzw. wtórnego zanieczyszczenia, w przypadku niedostatecznej czystości zastosowanej soli.
Tabela 1. Efektywność ekstrakcji fenoli z wody różnymi rozpuszczalnikami (stosunek fazy wodnej do fazy organicznej 25:1)
|
Związek |
Rozpuszczalnik |
|||
|
heksana) |
heksanb) |
toluenb) |
węglan dietylub) |
|
|
E [%] |
E [%] |
E [%] |
E [%] |
|
|
fenol |
– |
39 |
79 |
84 |
|
4-chlorofenol |
– |
78 |
90 |
99 |
|
4-chloro-3-metylofenol |
5 |
91 |
95 |
102 |
|
2,4-dichlorofenol |
34 |
92 |
94 |
101 |
|
2,4,6-trichlorofenol |
72 |
98 |
95 |
101 |
|
4-nitrofenol |
– |
13 |
85 |
98 |
|
2,3,4,6-tetrachlorofenol |
79 |
80 |
78 |
|
Wysoka efektywność ekstrakcji jest najczęściej jednym z głównych czynników decydujących o wyborze rozpuszczalnika. Jednakże wielokrotnie istotne mogą być także inne czynniki, jak również cel jaki chcemy osiągnąć w realizowanych oznaczeniach (np. szybkie badania przesiewowe lub dokładne określenie zawartości analitów). W badaniach zawartości zanieczyszczeń organicznych obecnych w wodach mineralnych sprzedawanych w butelkach plastikowych [20] do ekstrakcji stosowano heksan, a więc rozpuszczalnik niepolarny o stosunkowo słabych własnościach ekstrakcyjnych. O wyborze heksanu zdecydowały jednak inne jego cechy, a mianowicie pomijalna wzajemna rozpuszczalność z wodą oraz znaczna prężność par heksanu. Pierwsza cecha pozwala na ekstrakcję przy dużym stosunku faz oraz eliminuje ewentualną konieczność suszenia ekstraktu heksanowego. Natomiast druga cecha, duża lotność heksanu, pozwala na łatwą realizację dozowania próbek o dużej objętości. W realizowanych badaniach wód mineralnych ekstrakcję prowadzono w prosty sposób w kolbkach miarowych ze szklanym zamknięciem dla uniknięcia wprowadzenia zanieczyszczeń z polietylenowych korków. Stosunek fazy wodnej do fazy organicznej wynosił 100:1. Natomiast objętość dozowanej do układu chromatograficznego próbki wynosiła 250 μl i realizowana była za pomocą dozownika z programowaną temperaturą odparowania (PTV) [12,21]. W przeciwieństwie do próbek środowiskowych ekstrakty z wód mineralnych charakteryzują się bardzo dużą czystością (tzn. małą zawartością substancji nielotnych) i możliwe jest również stosowanie dozowania próbek o dużej objętości metodą do kolumny z ujściem par rozpuszczalnika. Na rysunku 1 przedstawiono przykładowy chromatogram 250 μl ekstraktu heksanowego zawierającego zanieczyszczenia wydzielone z wody mineralnej przy zastosowaniu uniwersalnego detektora płomieniowo-jonizacyjnego (FID), natomiast na następnym rysunku 2 chromatogram uzyskany przy zastosowaniu spektrometru mas. Zawartość dwóch składników oszacowana została na co najmniej 0,2 pbb. Jeden ze składników widocznych na chromatogramie zidentyfikowany został jako 2,4-di-tert-bytulo-fenol. Przedstawiona metoda pozwalała na bardzo szybkie oznaczanie zawartości zanieczyszczeń na bardzo niskim poziomie ppb przy zastosowaniu detektora FID.
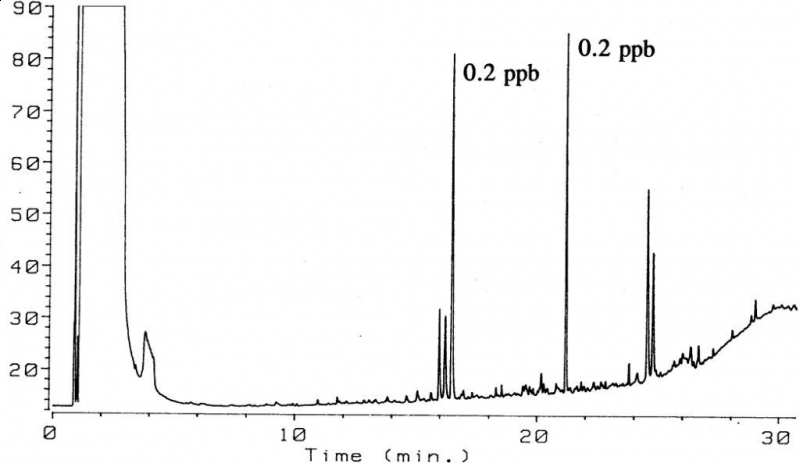
Rys. 1. Chromatogram 250 μl ekstraktu heksanowego wody mineralnej w opakowaniu z tworzywa sztucznego (podane wartości określają oszacowane zawartości zanieczyszczeń w wodzie).
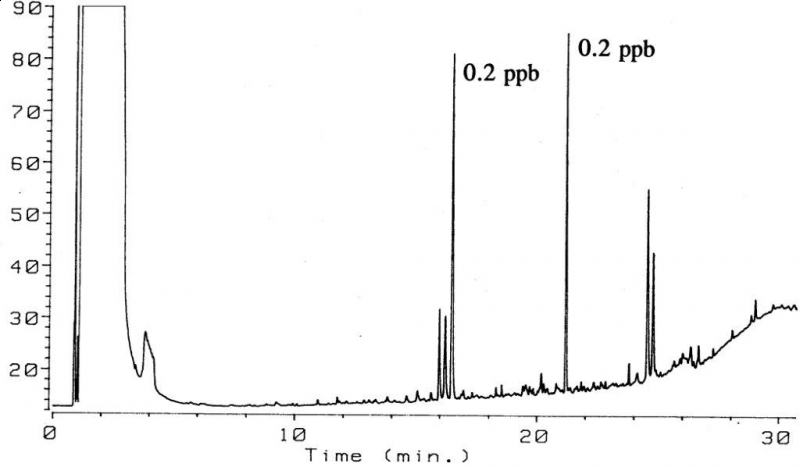
Rys. 2. Chromatogram GC-MS (zakres mas 45-800) 250 μl ekstraktu heksanowego zanieczyszczeń organicznych wody mineralnej.
Stosowanie małych ilości rozpuszczalnika w mikroekstrakcji ciecz-ciecz nie zapobiega ekstrakcji makrocząsteczek do fazy organicznej szczególnie w przypadku rzeczywistych próbek środowiskowych. Zastosowanie nieporowatej membrany polietylenowej lub polipropylenowej [22,23] eliminuje tę istotną wadę ekstrakcji ciecz-ciecz. Możliwe jest również użycie innych membran [24-26]. Na rysunku 3 przedstawiono fotografię prostego stanowiska do mikroekstrakcji ciecz-ciecz w obecności przegrody membranowej. Rozpuszczalnik umieszczono w handlowo dostępnych torebkach (o wymiarach 4 cm x 6 cm) z polietylenu o niskiej gęstości i całość zanurzono w mieszanej za pomocą mieszadła magnetycznego próbce wodnej.

Rys. 3. Fotografia stanowiska do mikroekstrakcji ciecz-ciecz w obecności przegrody membranowej.
W tabeli 2 przedstawiono przykładowe wyniki wydzielania fenoli z próbki wodnej, derywatyzowanych przed ekstrakcją bezpośrednio w wodzie do pochodnych acetylowych. Czas ekstrakcji wynosił 60 minut, a stosunek faz 100:1. Obecność hydrofobowej membrany zapobiegała przedostawaniu się wody do rozpuszczalnika. Uzyskano zadawalające wydzielenie dla większości fenoli przy zastosowaniu heksanu, toluenu lub tetrachlorometanu jako rozpuszczalników. W przypadku węglanu dietylu efektywność ekstrakcji była bardzo niska w przeciwieństwie do bezpośredniej ekstrakcji ciecz-ciecz. Spowodowane jest to brakiem możliwości wystąpienia oddziaływań pomiędzy węglanem dietylu a fenolami na granicy faz woda-rozpuszczalnik przedzielonej membraną nieporowatą. W tabeli zamieszczono również ubytki rozpuszczalnika, które wynosiły w od 3% dla węglanu dietylu do 12% dla heksanu.
Tabela 2. Efektywność ekstrakcji fenoli z wody różnymi rozpuszczalnikami w obecności nieporowate membrany (stosunek fazy wodnej do fazy organicznej 100:1, czas ekstrakcji 60 minut)
|
Związek |
Rozpuszczalnik |
|||
|
heksan |
tetrachloro-metan |
toluen |
węglan dietylu |
|
|
E [%] |
E [%] |
E [%] |
E [%] |
|
|
fenol |
5 |
7 |
18 |
<1 |
|
4-chlorofenol |
20 |
25 |
41 |
2 |
|
4-chloro-3-metylofenol |
34 |
36 |
59 |
5 |
|
2,4-dichlorofenol |
39 |
40 |
64 |
7 |
|
2,4,6-trichlorofenol |
60 |
53 |
76 |
18 |
|
4-nitrofenol |
2 |
4 |
15 |
– |
|
2,3,4,6-tetrachlorofenol |
68 |
54 |
77 |
27 |
|
ubytek rozpuszczalnika [%] |
12 |
7 |
9 |
3 |
Rysunek 4 przedstawia wpływ matrycy próbki wodnej (woda wodociągowa, woda rzeczna, woda powierzchniowa, woda gruntowa oraz ścieki bez osadów) na wydzielenie fenoli. Z przedstawionych na rysunku wyników można stwierdzić, że wpływ matrycy próbki na efektywność ekstrakcji jest pomijalny. Zaletą tej metody jest przede wszystkim uzyskanie czystego, pozbawionego makrocząsteczek ekstraktu, brak wody w fazie organicznej oraz bardzo łatwe rozdzielanie faz. Powyższa metoda znana jest w literaturze anglojęzycznej jako MALE – Membrane-Assisted Solvent Extraction [22,23].
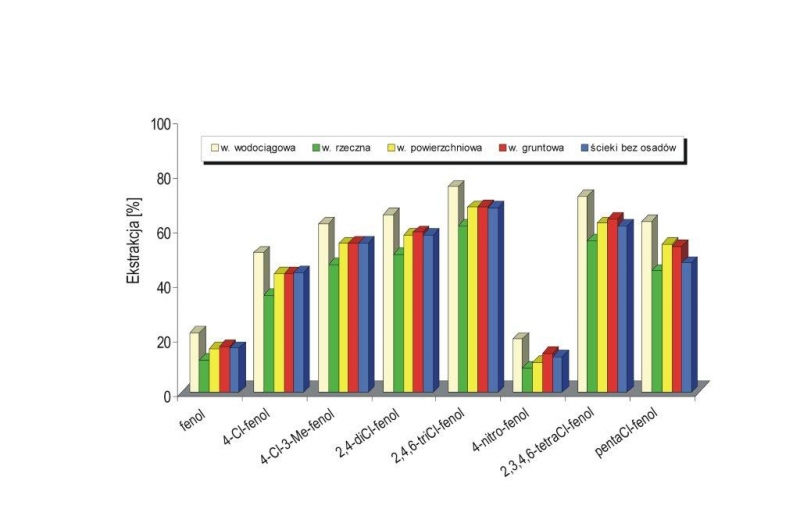
Rys. 4. Wpływ matrycy próbki wodnej (woda wodociągowa, różne wody powierzchniowe, ścieki bez osadu czynnego) na wydzielenie fenoli z wody w obecności przegrody membranowej.
Automatyzacja lub robotyzacja oznaczeń analitycznych, a szczególnie oznaczeń rutynowych, stanowi istotny kierunek rozwoju metod analitycznych. Wymaga to opracowania nowych metod przygotowania próbek lub miniaturyzację opracowanych już procedur w celu ich bezpośredniego połączenia z oznaczaniem końcowym [27,28]. Jedną z metod wydzielania analitów z próbek wodnych umożliwiającą bezpośrednie połączenie przygotowania próbki z oznaczaniem końcowym metodą kapilarnej chromatografii gazowej (cGC) lub wysokosprawnej chromatografii cieczowej (HPLC) jest ekstrakcja (sorpcja) do fazy stacjonarnej lub warstwy adsorpcyjnej umieszczonej w kapilarze [29,30]. Metoda ta występuje w literaturze anglojęzycznej pod wieloma nazwami, przy czym w ostatnim czasie preferowane jest określenie „in-tube SPME” [31-33]. Zdaniem autora niniejszego opracowania stosowanie nazwy CME Cappilary MicroExtraction byłoby bardziej adekwatne dla tej grupy metod. Ekstrakcja do fazy stacjonarnej kapilary może być realizowana w dwóch wariantach. W pierwszym opiera się na zasadzie całkowitego zatrzymania analitów w kapilarze [34]. W tym przypadku ważnym parametrem jest objętość przebicia kolumny. W drugim wariancie sorpcja może być prowadzona aż do osiągnięcia stanu równowagi i opiera się na zasadzie podziału analitów pomiędzy fazę stacjonarną a fazę wodną [30,35,36] w podobny sposób jak w konwencjonalnej metodzie mikroekstrakcji do fazy stacjonarnej SPME. Matematyczny model stanu równowagi procesu sorpcji do fazy stacjonarnej jest analogiczny z modelem opracowanym przez Loucha i in. [37] dla metody SPME. Zgodnie z tym modelem ilość m zatrzymanych na fazie polimerowej analitów w stanie równowagi jest proporcjonalna do ich stężenia początkowego Co w próbce wodnej i ściśle zależna od współczynnika podziału Kcs, co ilustruje poniższe równanie: gdzie: Vc – objętość fazy stacjonarnej, Vs – objętość próbki. Z powyższego równania wynika również, że ilość wydzielonej substancji (a co zatem idzie efektywność ekstrakcji) można zwiększyć dla danej próbki poprzez zwiększenie objętości fazy stacjonarnej oraz poprawę własności ekstrakcyjnych samej fazy stacjonarnej (to znaczy poprzez zwiększenie współczynnika podziału). Uwolnienie analitów z fazy stacjonarnej może być przeprowadzone poprzez desorpcję rozpuszczalnikiem lub desorpcję termiczną. W przypadku połączenia wydzielania w kapilarze z wysokosprawną chromatografią cieczową, ze zrozumiałych względów, desorpcja może zachodzić wyłącznie z użyciem rozpuszczalnika. Połączenie wydzielania w kapilarze z chromatografią gazową realizowane jest do wydzielania związków lotnych w znaczeniu chromatograficznym (tzw. substancje lotne VOC i średniolotne SVOC) z próbek wodnych lub gazowych [38]. W tych przypadkach substancje zatrzymane na filmie fazy stacjonarnej mogą być uwalniane w prosty sposób z kapilary w procesie termodesorpcji i wprowadzane do chromatografu gazowego. Desorpcja z filmu fazy stacjonarnej substancji średniolotnych (SVOC) wydzielonych z wody może być również realizowana przy użyciu rozpuszczalnika [29,30,34,35]. Wprowadzenie całej objętości rozpuszczalnika desorbującego anality do kolumny chromatograficznej realizowane jest poprzez dozowanie próbki o dużej objętości. Głównymi zaletami desorpcji rozpuszczalnikiem są: i) możliwość wyeliminowania wody z układu chromatograficznego, ii) zmniejszenie ryzyka degradacji oznaczanych związków, iii) zwiększenie trwałości filmu fazy stacjonarnej, iv) oczyszczanie kapilary rozpuszczalnikiem w procesie desorpcji, v) możliwość modyfikacji fazy stacjonarnej rozpuszczalnikiem. Schemat układu wydzielania analitów z próbek ciekłych poprzez sorpcję w kapilarze i ich desorpcję rozpuszczalnikiem przedstawiono na rysunku 5. Układ może być połączony bezpośrednio z systemem dozowanie próbki o dużej objętości chromatografu gazowego lub pracować jako samodzielny układ przygotowania próbek. Składa się z trzech zaworów wielodrożnych, pompy rozpuszczalnika desorbującego i rozpuszczalnika spęczniającego fazę stacjonarną oraz pompy perystaltycznej. Najważniejszym elementem układu jest odcinek kapilary z warstwą sorpcyjną (faza stacjonarna lub adsorbent) umieszczony na jednym z zaworów. Długość kapilary wynosi z reguły od 50-200 cm, a jej średnica wewnętrzna 0,53 mm. Możliwe jest stosowanie kapilar o mniejszej średnicy wewnętrznej, ale zmniejsza to znacznie ilość wydzielonych związków ze względu na mniejszą objętość fazy sorpcyjnej oraz zwiększa opory przepływu próbki przez kapilarę. Próbka umieszczana jest w jednej z fiolek. Powietrze pompowane przez pompę perystaltyczną wypycha próbkę z jednej fiolki poprzez kapilarę do drugiej. Po przełączeniu zaworu powietrze wprowadzane jest do drugiej fiolki powodując wypychanie próbki ponownie przez kapilarę z powrotem do pierwszej fiolki. Po kilku takich cyklach i usunięciu powietrzem próbki z kapilary przełączane są zawory do pozycji umożliwiającej desorpcję analitów rozpuszczalnikiem. Ekstrakt wprowadzany jest do chromatografu gazowego lub zbierany w naczyniu do dalszych oznaczeń. Druga pompa znajdująca się w układzie umożliwia spęcznianie fazy stacjonarnej odpowiednim rozpuszczalnikiem przed procesem wydzielania związków z próbki wodnej.
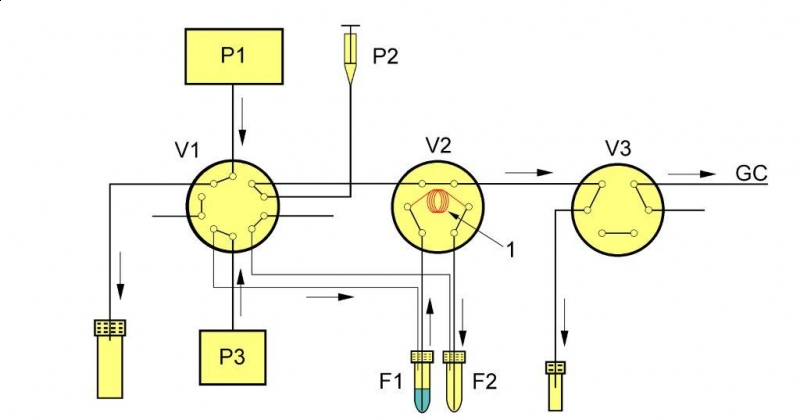
Rys. 5. Schemat układu wydzielania analitów z próbek ciekłych poprzez sorpcję w kapilarze (1 – kapilara ekstrakcyjna, V1, V2, V3 – zawory, P1 – pompa z heksanem, P2 – pompa z modyfikatorem, P3 – pompa perystaltyczna, F1, F2 –fiolki)
W wydzielaniu do fazy stacjonarnej lub warstwy adsorpcyjnej w kapilarze istotna jest zarówno efektywność wydzielania analitów z próbki jak również dynamika procesu sorpcji i desorpcji [30,36]. Na poniższych rysunkach przedstawiono dynamikę sorpcji wybranych fenoli do niepolarnej fazy stacjonarnej (Rys. 6) oraz do warstwy adsorpcyjnej (Rys. 7). W obu przypadkach sorpcja jest procesem stosunkowo szybkim i po około 15 minutach dynamicznego kontaktu próbki z warstwą sorpcyjną nie obserwuje się dalszego wydzielenia związków.
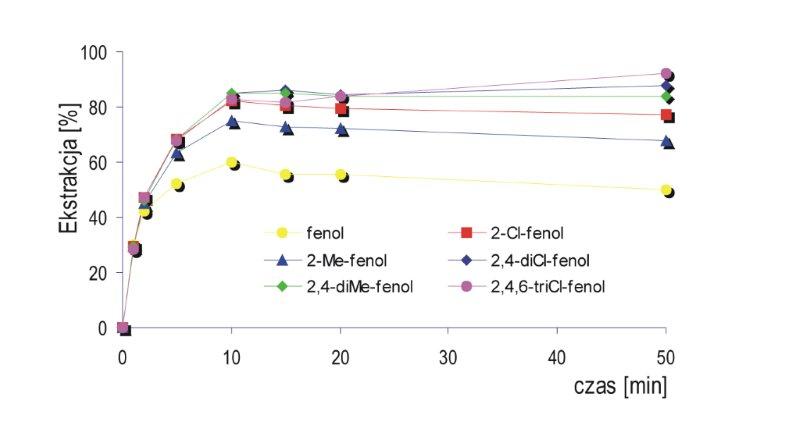
Rys. 6. Dynamika sorpcji fenoli do niepolarnej fazy stacjonarnej PDMS.
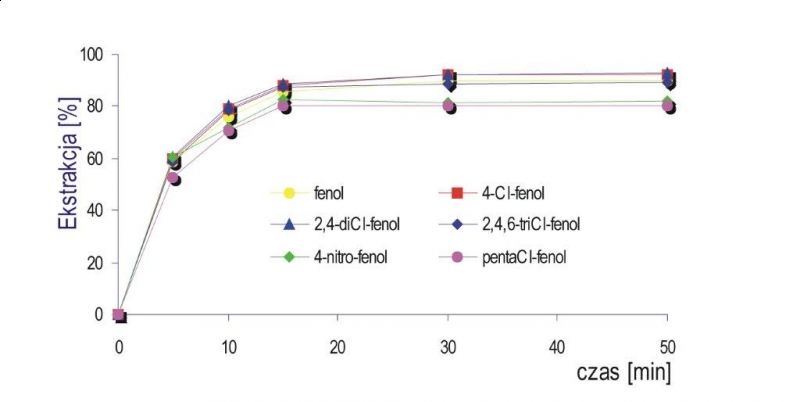
Rys. 7. Dynamika sorpcji fenoli do warstwy adsorpcyjnej PLOT Q.
W przedstawionym wcześniej opisie matematycznym wydzielania w kapilarze określono, że wzrost efektywności ekstrakcji dla danej próbki można uzyskać poprzez zwiększenie objętości fazy stacjonarnej oraz zwiększenie współczynnika podziału, czyli zmianę własności ekstrakcyjnych samej fazy np. poprzez zwiększenie jej polarności. Na rysunku 8 przedstawiono wpływ polarności faz stacjonarnych na efektywność ekstrakcji fenoli. Zastosowane zostały: niepolarna faza polidimetylosiloksanowa (CP-Sil5CB) oraz bardziej polarne fazy Q-17 oraz Q-225. Pierwsza to polidimetylosiloksan modyfikowany grupami fenylowymi (w ilości 50%) – wykazującą słabo polarne właściwości, a druga to polidimetylosiloksan modyfikowany grupami cyjanopropylofenylowymi (w ilości 50%) – charakteryzującą się średnią polarnością. Najwyższe wydzielenie uzyskano na najbardziej polarnej kolumnie kapilarnej Q-225, natomiast najniższe na niepolarnej kolumnie CP-Sil5CB. Faza stacjonarna Q-225 (z grupami cyjanopropylofenylowymi), jako jedyna wykazała zdolność zatrzymania 4-nitrofenolu i pozwalała na czterokrotne wyższe wydzielenie w porównaniu z fazą niepolarną dla szeregu związków tj.: 4-metylofenolu, 3- i 4-chlorofenolu, 2,3-dimetylofenolu, 4-chloro-3-metylofenolu.
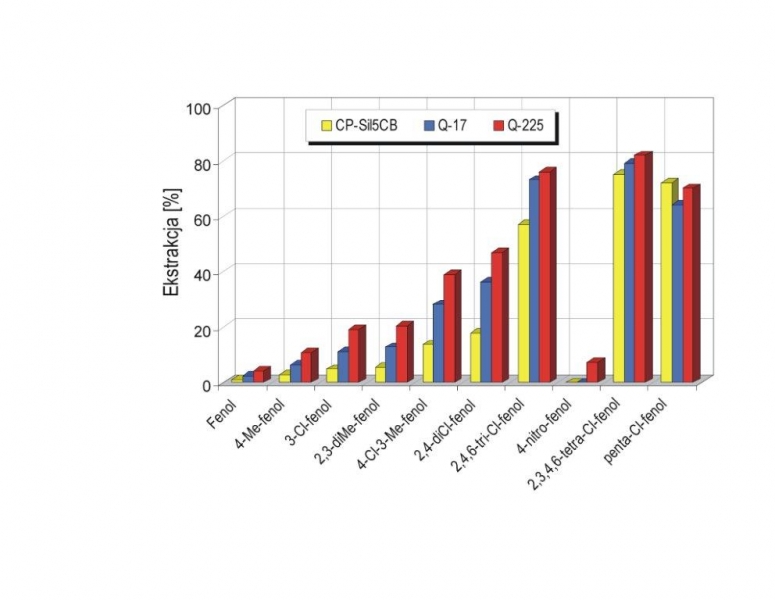
Rys. 8. Wpływ polarności faz stacjonarnych na efektywność ekstrakcji fenoli.
Zmianę własności sorpcyjnych kapilary można uzyskać również poprzez spęcznienie fazy odpowiednim rozpuszczalnikiem np.: heksanem, toluenem lub tetrachlorometanem. Rozpuszczalnik spęczniający odgrywa jednak tutaj podwójną rolę: powoduje zmianę własności fazy stacjonarnej oraz zwiększa objętość fazy stacjonarnej. Wpływ spęcznienia fazy stacjonarnej rozpuszczalnikiem przedstawiono na chromatogramach (Rys. 9). Chromatogram B obrazujące wpływ spęcznienia heksanem na wydzielanie fenoli, natomiast chromatogram C toluenem. Dla porównania zamieszczono również chromatogram uzyskany po wydzieleniu fenoli na fazie niespęcznionej (część A) – na której obserwuje się wydzielenie tri-, tetra- i penta- chlorofenoli na poziomie 30-40%. Po spęcznieniu fazy heksanem wydzieleniu uległy wszystkie analizowane fenole: 2- i 4-nitrofenole na poziomie 10%, fenol około 16%, a pozostałe w przedziale 30-90%. Natomiast po spęcznieniu fazy toluenem efektywność wydzielenia fenoli wynosiła 50-90%.
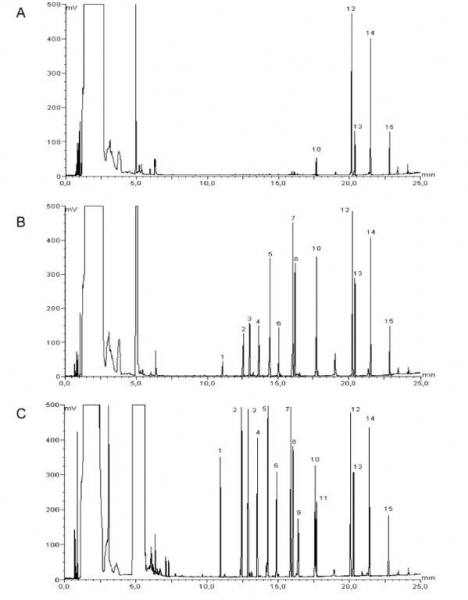
Rys. 9. Chromatogram fenoli zatrzymanych na niespęcznianej fazie stacjonarnej HP-1 (A), na fazie spęcznianej heksanem (B) i na fazie spęcznianej toluenem (C) (1 – fenol; 2 – 2-metylofenol; 3 – 3-metylofenol; 4 – 2-chlorofenol; 5 – 2,4-dimetylofenol; 6 – 2-bromofenol; 7 – 4-chloro-2-metylofenol; 8 – 2,4-dichlorofenol; 9 – 2-nitrofenol; 10 – 2,4,6-trichlorofenol; 11 – 4-nitrofenol; 12 – n-heksadekan; 13 – 2,3,4,6-tetrachlorofenol; 14 – n-heptadekan; 15 – pentachlorofenol).
Bardzo efektywne wydzielanie fenoli uzyskano dla kolumny z warstwą adsorpcyjną, którą stanowił kopolimer diwinylobenzenu i styrenu (HP Plot Q o grubości warstwy 40 μm). Uzyskane wyniki wydzielania wybranych fenoli na niemodyfikowanej oraz modyfikowanej polidimetylosiloksanem warstwie adsorbentu przedstawiono w tabeli 3. Dla porównania zamieszczono również wyniki ekstrakcji do niepolarnej fazy PDMS (CP-Sil5CB) spęcznianej toluenem. Sorpcja do niemodyfikowanej warstwy PLOT Q wynosiła 80-90% dla wszystkich badanych fenoli. Pokrycie warstwy PLOT Q polidimetylosiloksanem w celu zwiększenia jej trwałości nie wpływa zasadniczo na efektywność ekstrakcji. Dodatkowe spęcznienie zmodyfikowanej warstwy rozpuszczalnikiem obniża nieznacznie tylko wydzielanie fenolu i nitrofenolu.
Tabela 3. Efektywność wydzielania fenoli do kapilary z warstwą adsorpcyjną PLOT Q
|
Związek |
Kapilara ekstrakcyjna |
|||
|
CP-Sil 5 CB toluen |
HP Plot Q |
HP Plot Q 4,3mg PDMS |
HP Plot Q 4,3mg PDMS heksan |
|
|
E [%] |
E [%] |
E [%] |
E [%] |
|
|
fenol |
28 |
86 |
75 |
37 |
|
4-chlorofenol |
66 |
87 |
82 |
73 |
|
4-chloro-3-metylofenol |
80 |
89 |
85 |
85 |
|
2,4-dichlorofenol |
81 |
89 |
84 |
85 |
|
2,4,6-trichlorofenol |
83 |
87 |
83 |
87 |
|
4-nitrofenol |
35 |
87 |
84 |
52 |
|
2,3,4,6-tetrachlorofenol |
74 |
77 |
71 |
76 |
|
pentachlorofenol |
73 |
80 |
73 |
79 |
Przygotowanie próbki przez wydzielanie w kapilarze z fazą stacjonarną zastosowano do oznaczeń fenoli w próbkach środowiskowych. Wydzielanie połączono z oznaczaniem metodą kapilarnej chromatografii gazowej dozując część ekstraktu z kapilary (100 μl z 200 μl ekstraktu) metodą do kolumny z tzw. ujściem par rozpuszczalnika [36]. Poziom wykrywalności metody off-line wynosił od 0,014 do 0,04 μg/l przy zastosowaniu detektora FID. Połączenie opracowanej metody przygotowania próbek bezpośrednio z oznaczaniem metodą chromatografii gazowej tzw. układ on-line umożliwia wprowadzenie całego ekstraktu do układu chromatograficznego i pozwala na uzyskanie nieznacznie niższego poziomu wykrywalności. Bezpośrednie połączenie on-line eliminuje ponadto dodatkowe operacje w trakcie realizacji przygotowania próbki, co zapobiega ewentualnemu zanieczyszczeniu próbki. Chromatogram uzyskany dla bezpośrednich oznaczeń fenoli w wodzie na poziomie 5 μg/l przedstawiono na rysunku 10. Szeroki pik toluenu spęczniającego fazę stacjonarną w kapilarze nie przeszkadza w rozdziale fenoli i ich ocenie ilościowej. Stwierdzono również, że stosując kapilarę z fazą stacjonarną i desorpcję rozpuszczalnikiem możliwe jest wykonanie setek oznaczeń bez istotnych zmian własności analitycznych metody.
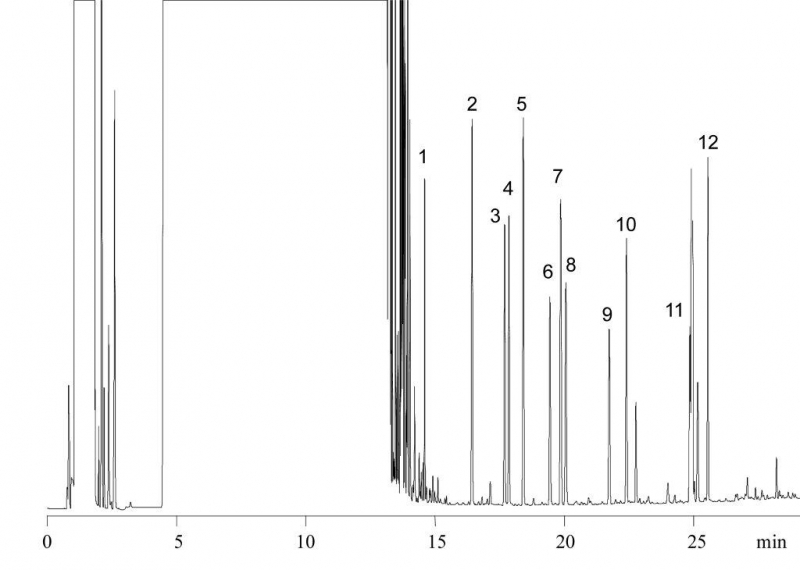
Rys. 10. Chromatogram fenoli (stężenie w wodzie 5 μg/l) wydzielanych poprzez sorpcję do fazy stacjonarnej w kapilarze (faza CP-Sil5CB spęczniana toluenem, dł. kapilary 200 cm, objętość próbki 8 ml) i oznaczanych bezpośrednio metodą chromatografii gazowej (1 – fenol; 2,4-metylofenol; 3 – 3-chlorofenol; 4 – 4-chlorofenol; 5 – 2,3-dimetylofenol; 6 – 4-metoksyfenol; 7 – 4-chloro-3-metylofenol; 8 – 2,4-dichlorofenol; 9 –2,4,6-trichlorofenol; 10 – 4-nitrofenol; 11 – 2,3,4,6- tetrachlorofenol; 12 – pentachlorofenol).
Przedstawione w pracy metody przygotowania próbek określone jako metody niekonwencjonalnych posiadają wiele cech wymaganych od współczesnych metod analitycznych i mogą być z powodzeniem stosowane w codziennej praktyce laboratoryjnej na równi z uznanymi metodami konwencjonalnymi.
Praca zrealizowana częściowo w ramach DS–32/139/08.
Literatura:
1. R.E. Majors, LC-GC, 4 (1991) 10. 2. R.E. Majors, LC-GC, 20 (2002) 1098. 3. D.E. Raynie, Anal. Chem., 76 (2004) 4659. 4. D.E. Raynie, Anal. Chem., 78 (2006) 3997. 5. Praca zbiorowa pod red. P. Konieczki i J. Namieśnika, Ocena i kontrola jakości wyników pomiarów analitycznych, WNT Warszawa, 2007. 6. J. Namieśnik, J. Sep. Sci., 24 (2001) 151. 7. W. Wardencki, J. Curyło, J. Namieśnik, Pol. J. Environ. Stud., 14 (2005) 389. 8. E. Baltussen, P. Sandra, F. David, C.A. Cramers, J. Microcol. Sep. 11 (1999) 737. 9. B. Buszewski, T. Ligor, LC●GC Europe, 15 (2002) 92. 10. Y. He, H.K. Lee, Anal. Chem., 69 (1997) 4634. 11. D.A. Lambropoulou, T.A. Albanis, J. Chromatogr. A, 1072 (2005) 55. 12. J. Staniewski, H.-G. Janssen, C.A. Cramers, J.A. Rijks, J. Microcol. Sep., 4 (1992) 331. 13. G.R. van der Hoff, R.A. Baumann, U.A.Th. Brinkman, P. van Zoonen, J. Chromatogr., 644 (1993) 367. 14. J. Teske, J. Efer, W. Engewald, Chromatographia, 47 (1998) 35. 15. A. Urbańczyk, J. Staniewski, W. Apostoluk, J. Szymanowski, Chem. Anal. (Warsaw), 47 (2002) 669. 16. J. Olejniczak, J. Staniewski, J. Szymanowski, Anal. Chim. Acta, 535 (2005) 251. 17. M. Rezaee, Y. Assadi, M.-R.M. Hosseini, E. Aghaee, F. Ahmadi, S. Berijani, J. Chromatogr. A, 1116 (2006) 1. 18. N. Fattahi, S. Samadi, Y. Assadi, M.-R. M. Hosseini, J. Chromatogr. A, 1169 (2007) 63. 19. G. Wie, Y. Li, X. Wang, J. Sep. Sci., 30 (2007) 3262. 20. J. Staniewski, w: J. Siepak, Metody pobierania i przygotowania próbek wody, ścieków i osadów do analiz fizyczno-chemicznych, ISBN 83-908178-0-2, Poznań 1997, s. 69. 21. J. Staniewski, w: B. Buszewski, Nowoczesne metody analityczne w kontroli i monitoringu środowiska, Materiały II Ogólnopolskiego Seminarium Chromatograficznego, ISBN 83-231-0667-3, Toruń 1995, s. 106. 22. B. Hauser, M. Schellin, P. Popp, Anal. Chem., 76 (2004) 6029. 23. M. Schellin, P. Popp, J. Chromatogr. A, 1072 (2005) 37. 24. M. Jánská, S.J. Lehotay, K. Maštovská, J. Hajšlová, T. Alon, A. Amirav, J. Sep. Sci., 29 (2006) 66. 25. Y. Shen, J.Å. Jőnssen, L. Mathiasson, Anal. Chem., 70 (1998) 946. 26. C. Basheer, A.A. Alnedhary, B.S.M. Rao, S. Valliyaveettil, H.K. Lee, Anal. Chem., 78 (2006) 2853. 27. J. Staniewski, w: B. Buszewski, Ekoanalityka w chemii środowiska, Materiały V Ogólnopolskiego Sympozjum Chromatograficznego, ISBN 83-902584-0-4, Toruń 1998, s. 47. 28. J. Staniewski, w: B. Buszewski, Chromatografia i inne techniki separacyjne u progu XXI wieku, Materiały VI Ogólnopolskiego Sympozjum Chromatograficznego, ISBN 83-88245-00-7, Toruń 1999, s. 171. 29. H.G.J. Mol, H-G. Janssen, C.A. Cramers, J. High Resol. Chromatogr., 16 (1993) 413. 30. J. Olejniczak, J. Staniewski, J. Szymanowski, Anal. Chim. Acta, 497 (2003) 199. 31. R. Eisert, J. Pawliszyn, Anal. Chem., 69 (1997) 3140. 32. H. Kataoka, H.L. Lord, J. Pawliszyn, J. Chromatogr. A, 880 (2000) 35. 33. H. Kataoka, Anal. Bioanal. Chem., 373 (2002) 31. 34. H.G.J. Mol, J. Staniewski, H-G. Janssen, C.A. Cramers, R.T. Ghijsen, U.A.Th. Brinkman, J. Chromatogr. A, 630 (1993) 201. 35. W.M. Mullett, P. Martin, J. Pawliszyn, Anal. Chem., 73 (2001) 2383 36. J. Olejniczak, J. Staniewski, Anal. Chim. Acta, 588 (2007) 64. 37. D. Louch, S. Motlagh, J. Pawliszyn, Anal.Chem., 64 (1992) 1187. 38. C. Aguilar, H-G. Janssen, C.A. Cramers, J. Chromatogr. A, 867 (2000) 207.
*Jacek Staniewski, Politechnika Poznańska, Instytut Technologii i Inżynierii Chemicznej pl. M. Skłodowskiej-Curie 2, 60-965 Poznań; e-mail: jacek.staniewski@put.poznan.pl(link sends e-mail)
