Zastosowanie spektroskopii NMR do badania chininy
Dorota Duczyńska – Szewczyk
Chinina jest substancją chemiczną stosowaną m in. w medycynie i przemyśle spożywczym. Ma postać białego proszku a pozyskiwana jest z kory drzewa chinowego rosnącego w górach Ameryki Południowej. Chinina jest organicznym związkiem chemicznym z grupy alkaloidów (podobnie jak kokaina i morfina). Charakteryzuje się intensywnie gorzkim smakiem, dlatego wykorzystywana jest do produkcji gorzkawych napojów orzeźwiających zwanych tonikami. Jest słabo rozpuszczalna w wodzie, natomiast dobrze rozpuszcza się rozpuszczalnikach organicznych.
Chininę zastosowano z sukcesem jako pierwszy lek na malarię – chorobę wywołaną przez pierwotniaki. Choć w walce z tą groźną chorobą odznacza się bardzo wysoką skutecznością, wywołuje przy okazji sporo skutków ubocznych – z tego względu z czasem wyparły ją inne, mniej szkodliwe substancje, głównie chlorochina.
Substancja ta jest wpisana na listę EML publikowaną od 1977 roku przez WHO (World Health Organization) i jest nadal stosowana w leczeniu trudniejszych przypadków malarii.
Chinina to nie tylko najskuteczniejszy lek na malarię, który zabija pasożyty wywołujące chorobę. Ponadto działa przeciwgorączkowo i przeciwbólowo. W medycynie wykorzystywana jest też jako lek przeciw-arytmiczny, gdyż zmniejsza pobudliwość oraz przewodnictwo mięśnia serca, zapobiegając nieprawidłowym pobudzeniom. Chinina zwalnia pracę serca oraz zmniejsza siłę jego skurczu, dlatego doskonale sprawdza się jako panaceum na napadowe migotanie i trzepotanie przedsionków.
Substancja z kory drzewa chinowego działa pobudzająco na wydzielanie soków trawiennych, dlatego jest niekiedy stosowana jako środek usprawniający trawienie. Wykorzystywana jest też w leczeniu skurczów łydek, gośćca stawowego, przeziębień oraz foto-dermatoz, czyli zmian skórnych wywołanych uczuleniem na światło. Z uwagi na szerokie zastosowanie chininy oraz jej własności substancja ta często jest przedmiotem badań naukowych.
Badanie chininy metodą spektroskopii NMR pokazano na kilku poniższych przykładach stosując eksperymenty jedno i dwuwymiarowe.
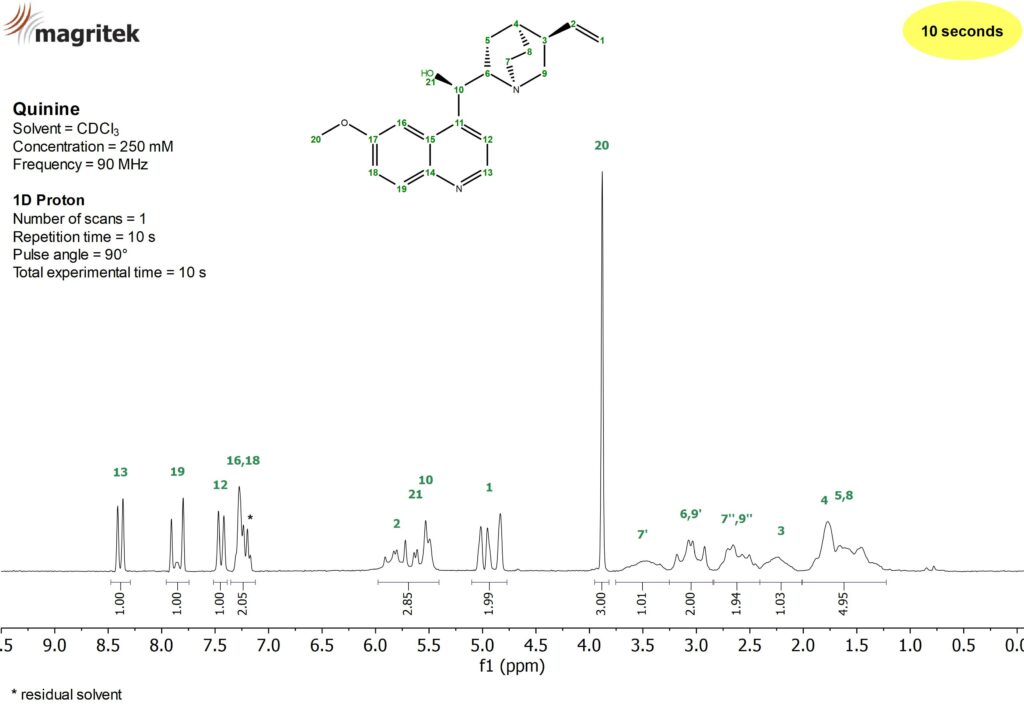
Rysunek 1. Eksperyment jednowymiarowy, widmo 1H NMR dla próbki 250 mM chininy w CDCl3 uzyskane w pojedynczym skanowaniu na aparacie Spinsolve 90 MHz przy czasie akwizycji 10 sekund.
Eksperyment jednowymiarowy 13C
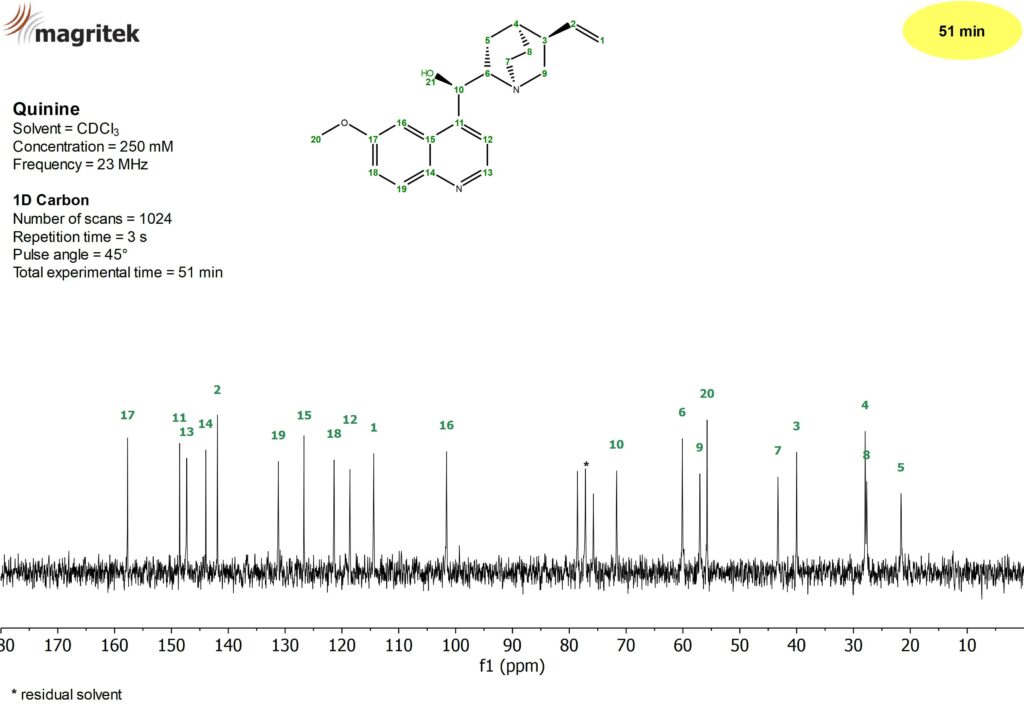
Rysunek 2. Widmo 13C NMR dla próbki 250 mM chininy w CDCl3 uzyskane na aparacie Spinsolve 90 MHz w czasie 51 minut.
Zastosowano transfer polaryzacji NOE od spinów 1H i 13C z szerokopasmowym odprzęganiem 1H. Badanie 1D 13C z zastosowaniem efektu NOE jest czułe dla wszystkich jąder 13C w próbce. Wyraźnie pokazuje wszystkie spodziewane rezonanse, jednocześnie eliminując informacje o powiązaniach wzajemnych między tymi jądrami.
Eksperyment dwuwymiarowy COSY
Eksperyment 2D COSY pozwala na identyfikację sprzężonych jąder 1H. Sygnały dla tych jąder pojawią się poza diagonalną na widmach korelacyjnych.
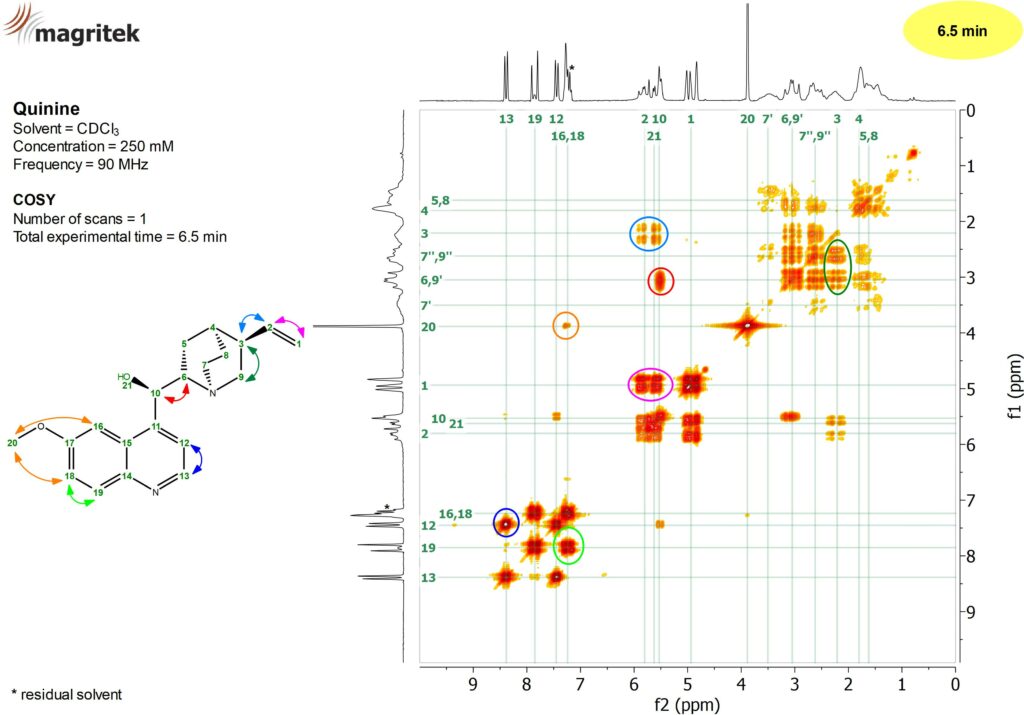
Rysunek 3: Eksperyment 1H 2D COSY dla próbki 250 mM chininy w CDCl3 uzyskany w czasie 6,5 minuty na aparacie Spinsolve 90 MHz.
Na rysunku można zaobserwować liczne piki korelacyjne. Przykładowo, proton w pozycji 13 sprzęga się z protonem z pozycji 12 (zaznaczono na granatowo), protony oznaczone cyframi 16 i 18 sprzęgają się z protonem 20 (kolor pomarańczowy), proton oznaczony 18 sprzęga się z protonem 19 (kolor jasnozielony), proton 2 sprzęga się z protonami 1 (kolor różowy) i 3 (jasnoniebieski). Ponadto można zaobserwować sprzężenie pomiędzy protonami 3 i 9 (oznaczone kolorem ciemnozielonym) i protonami 6 i 10 (zaznaczonymi na czerwono).
Eksperyment dwuwymiarowy 2D HSQC-ME
Eksperyment HSQC jest szeroko stosowanym eksperymentem korelującym jądra 1H sprzężone jednym wiązaniem z jądrami 13C. Aparat Spinsolve umożliwia wykonywanie eksperymentów w trybie HSQC-ME (multiplicity edited). To rozszerzenie eksperymentu HSQC pozwala na wyraźną edycję sekwencji DEPT-135, co jest wykorzystywane do rozróżnienia sygnałów grup CH2 (kolor niebieski) od grup CH i CH3 (kolor czerwony).
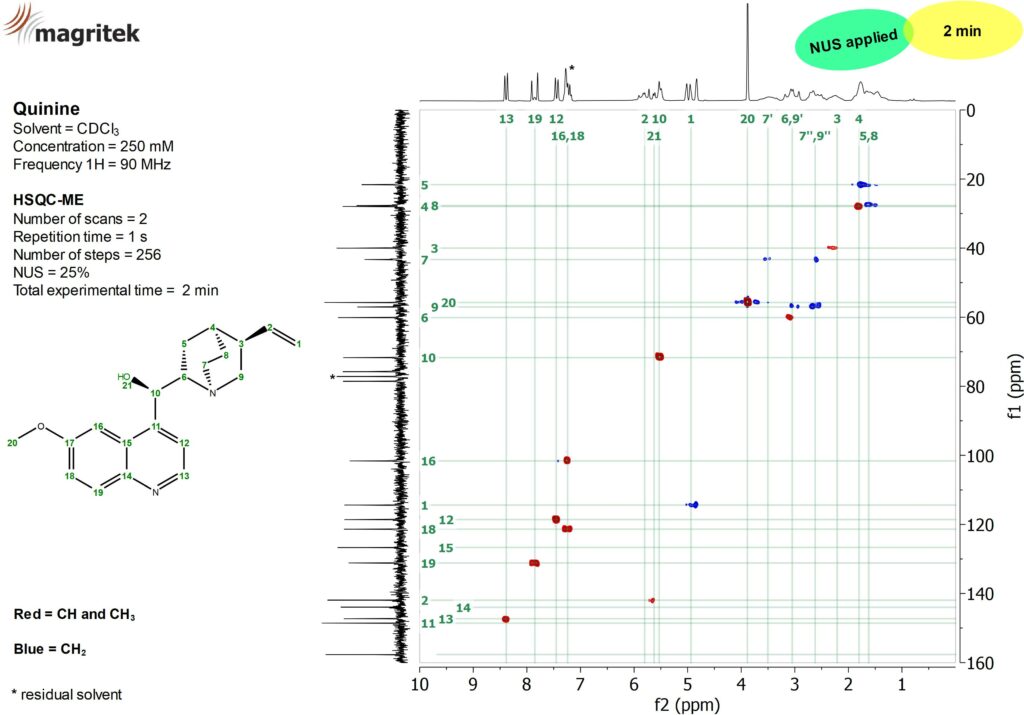
Rysunek 4: Widmo HSQC-ME dla próbki 250 mM chininy w CDCl3 uzyskane w czasie 2 minut. Czas pomiaru zoptymalizowano stosując próbkowanie niejednorodne NUS (non uniform sampling).
Eksperyment dwuwymiarowy HMBC
W celu uzyskania informacji korelacjach 1H-13C dalekiego zasięgu poprzez dwa lub trzy wiązania można wykorzystać eksperyment dwuwymiarowy Heteronuclear Multiple Bond Correlation (HMBC).
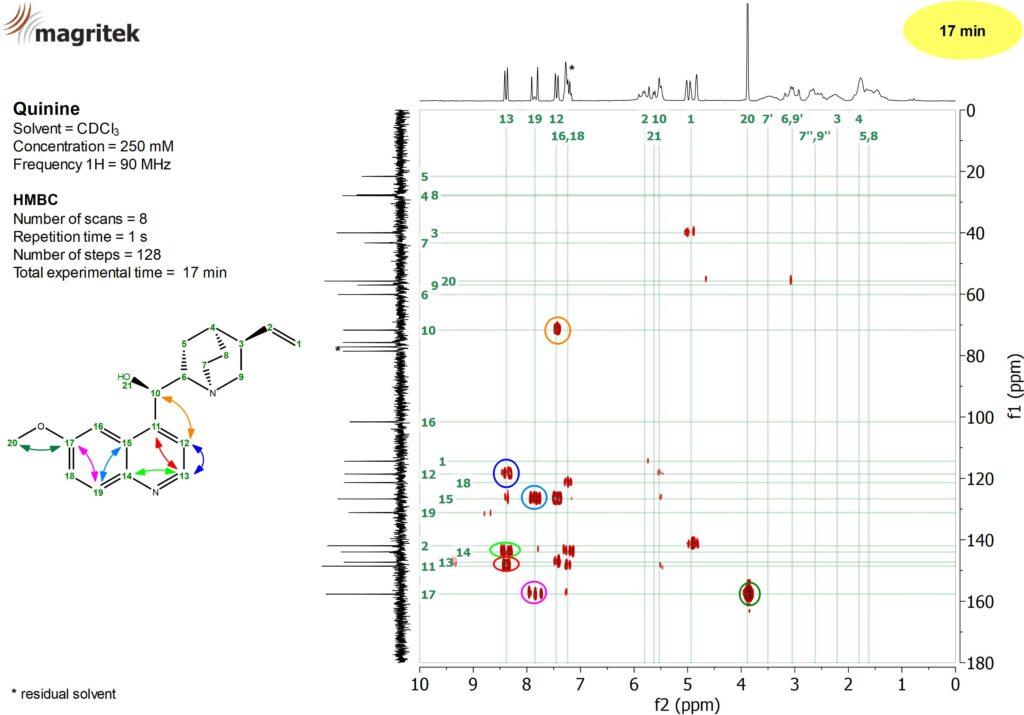
Rysunek 5. Widmo HMBC dla próbki chininy 250 mM uzyskane w czasie 17 minut z wykorzystaniem aparatu Spinsolve 90 MHz przedstawiono na rysunku obok. Widmo to przedstawia sprzężenia wiązań dalekiego zasięgu pomiędzy jądrami 1H i 13C.
Przykładowe korelacje dalekiego zasięgu przedstawione na rysunku 5: sprzężenia protonu 13 z jądrami węgla 12 (ciemnoniebieski), 14 (jasnozielony) i 11 (czerwony), jak też sprzężenia protonu 19 z jądrami węgla 15 (jasnoniebieski) i 17 (różowy), sprzężenie protonu 12 z węglem 10 (pomarańczowy) i protonów 20 z węglem 17 (ciemnozielony). Eksperyment pokazuje też korelację z czwartorzędowymi jądrami węgla.

