Topnienie i rozkład witaminy C
Dr Markus Schubnell
W tym artykule opisano, jak badaliśmy topnienie i stabilność termiczną witaminy C (kwasu askorbinowego) za pomocą pomiarów DSC i TGA. Okazuje się, że witamina C rozkłada się przed stopieniem lub po, zależnie od szybkości ogrzewania: przy niewielkiej szybkości ogrzewania rozkład zaczyna się przed stopieniem, przy dużej − po stopieniu.
Wstęp
Dla wielu krystalicznych związków organicznych nie można podać dokładnego punktu topnienia. Powodem tego jest fakt, że rozkład zaczyna następować tuż przed topnieniem lub w trakcie. Próbka nie jest już wtedy czysta. Prowadzi to do poszerzenia piku topnienia i obniżenia temperatury onset piku topnienia. W tym artykule przedstawiamy to zachowanie na przykładzie witaminy C. Witamina C jest znana pod nazwą chemiczną jako kwas askorbinowy. Kwas askorbinowy może występować w czterech
postaciach stereoizomer ycznych. W organizmie człowieka biologicznie aktywny jest tylko tzw. kwas
L−(+)-askorbinowy. W Unii Europejskiej znajduje się na liście dodatków do żywności (E 300).
Zalecane zapotrzebowanie dla dorosłego człowieka wynosi około 100 mg/dzień. Niedobór witaminy
C prowadzi do szkorbutu. Do końca osiemnastego wieku była to najczęstsza przyczyna śmierci w długich podróżach morskich. W branży spożywczej witamina C jest często stosowana jako antyoksydant.
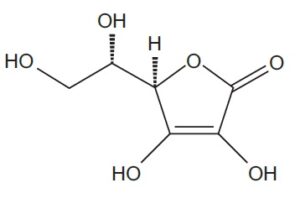 Rysunek 1. Wzór strukturalny kwasu askorbinowego.
Rysunek 1. Wzór strukturalny kwasu askorbinowego.
Szczegóły eksperymentu
Pomiary przeprowadzono za pomocą urządzenia DSC 3+ sprzężonego z systemem kamer mikroskopowych. Wykonano również pomiary z wykorzystaniem urządzenia TGA/DSC 3+
wyposażonego w czujnik DTA. Próbki zmierzono przy różnych szybkościach ogrzewania w tyglach aluminiowych o pojemności 40 μl, z wyjątkiem pomiarów DSC, w których zastosowano szybkości ogrzewania powyżej 20 K/min. W tym przypadku jako tygle zastosowano pokrywy tygli aluminiowych
o pojemności 20 μl. Pomiary DSC przeprowadzono w statycznym powietrzu, a pomiary TGA /DSC 3+
w powietrzu o prędkości przepływu 30 ml/min. Witamina C (CAS 50-81-7) pochodziła z firmy Sigma Aldrich.
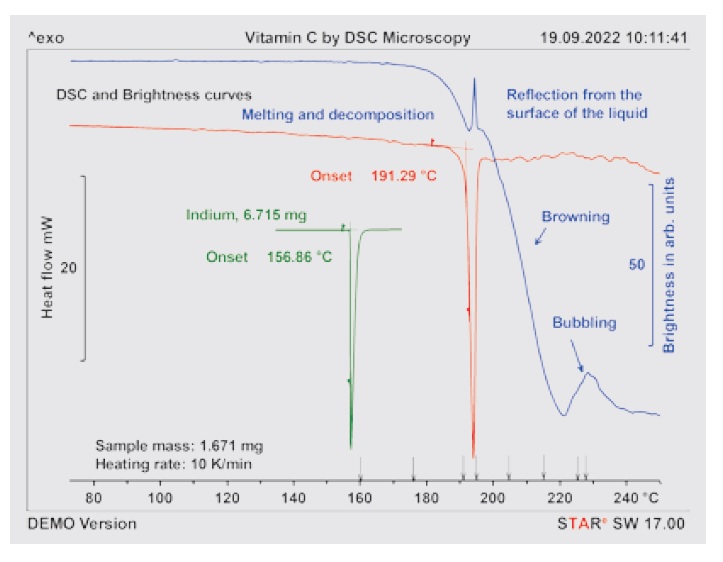
Rysunek 2. Krzywe DSC i jasności próbki witaminy C zmierzone przy szybkości ogrzewania 10 K/min.
Wyniki
Na rysunku 1 p rzedstawiono krzywą topnienia DSC witaminy C (krzywa czerwona) wraz z „krzywą jasności” (krzywa niebieska) obliczoną na podstawie zdjęć wykonanych przez kamerę podczas ogrzewania próbki. Dla każdego obrazu obliczono średnią jasność pozorną próbki. W temperaturze pokojowej witamina C ma postać białego proszku. Jasność próbki jest więc na początku stosunkowo wysoka i stała. Jednak od około 175°C jasność powoli maleje. Po zakończeniu eksperymentu w tyglu pozostaje ciemnobrązowo-czarny osad, a jasność osiąga stały niski poziom. Jasność na krótko wzrasta
podczas topnienia w temperaturze około 194°C. Wynika to z bezpośredniego odbicia światła od powierzchni próbki cieczy. Na zdjęciach wykonanych w wyższych temperaturach widać, że
próbka staje się brązowa i odbarwiona do około 220°C. Od około 220°C powstają pęcherzyki gazu, a światło odbite od pęcherzyków powoduje krótkotrwały wzrost jasności. Na rysunku 2 przedstawiono stosowne obrazy próbki w różnych temperaturach (oznaczone strzałkami na rysunku 1). Krzywa jasności
i zdjęcia dowodzą, że przy 10 K/min witamina C już zaczyna się rozkładać przed topnieniem.
Temperatury onset procesów rozkładu zależą od szybkości ogrzewania. Na rysunku 3 przedstawiono kilka krzywych DSC zmierzonych przy różnych szybkościach ogrzewania: większy wykres po lewej stronie
przedstawia krzywe DSC zmierzone przy 2, 5, 10 i 20 K/min, a mniejszy wykres po prawej krzywe zmierzone przy 50, 100 i 200 K/min. Te ostatnie pomiary były wykonywane z użyciem pokrywek tygli aluminiowych o pojemności 20 μl jako tygli w celu zmniejszenia stałej czasowej sygnału. Krzywe zostały znormalizowane do masy próbki i szybkości ogrzewania.
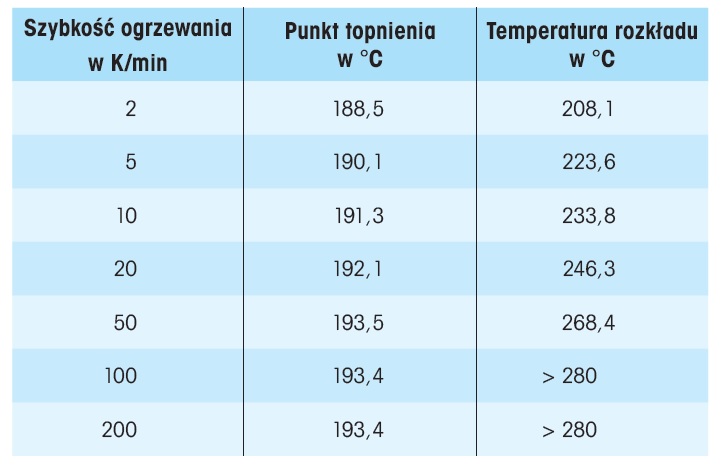
Tabela 1. Punkty topnienia (onset) i temperatury rozkładu (pik) witaminy C zmierzone przy różnych szybkościach ogrzewania.
Można zauważyć, że wraz ze wzrostem szybkości ogrzewania temperatura piku topnienia przesuwa się do wyższej temperatury. Ponadto krzywa DSC zmierzona przy 2 K/min wykazuje wyraźne ramię przed pikiem topnienia, co wskazuje, że zachodzi endotermiczna reakcja rozkładu. Przy małych szybkościach ogrzewania witamina C jest silniej zanieczyszczona produktami rozkładu przed topnieniem. Wyjaśnia to pozorną zależność piku topnienia od szybkości ogrzewania. Kształt piku topnienia wskazuje również, że ilość zanieczyszczeń wzrasta przy niższych szybkościach ogrzewania: w przypadku czystych materiałów krzywa DSC podczas topnienia powinna być linią prostą. Tak jest w przypadku krzywych zmierzonych przy 50, 100 i 200 K/min. Przy tych szybkościach ogrzewania temperatura początku procesu topnienia jest również niezależna od szybkości ogrzewania, czego należałoby się spodziewać po czystym materiale. Temperatury onset (topnienia) i piku (rozkładu) przy różnych szybkościach ogrzewania zestawiono w tabeli 1. Na rysunku 4 przedstawiono te zależności graficznie; oś x (szybkość ogrzewania) jest wykreślona w skali logarytmicznej. Gdyby przyczyna widocznej zależności temperatury topnienia od szybkości ogrzewania była wynikiem nieprawidłowego opóźnienia tau, należałoby oczekiwać wyraźnej krzywej, a nie linii prostej. Przy szybkości ogrzewania większej niż 50 K/min nie obserwuje się już pozornej zależności temperatury onset od szybkości ogrzewania. „Prawdziwa” temperatura topnienia witaminy C wynosi zatem 193,5 ±0,3°C. Fakt, że witamina C zaczyna się rozkładać przed topnieniem przy niskich
szybkościach ogrzewania, został również wykazany w eksperymencie TGA. Na rysunku 5 przedstawiono kilka pomiarów TGA wykonanych przy szybkościach ogrzewania 2, 10, 25, 50 i 100 K/min. Na górnym wykresie po prawej stronie przedstawiono zmierzone krzywe TGA. Poniżej przedstawiono zmierzone jednocześnie krzywe TGA/DSC i DTG dla szybkości ogrzewania 25, 50 i 100 K/min. Przy tych szybkościach ogrzewania rozkład wyraźnie rozpoczyna się powyżej temperatury topnienia. Na wykresie
po lewej stronie rysunku 5 przedstawiono krzywe DSC (linie kropkowane) zmierzone przy 2 i 10 K/min wraz z krzywymi DTG (linie ciągłe). Przy 2 K/min krzywa DTG kieruje się w dół od około 175°C, wskazując w ten sposób utratę masy. Topnienie rozpoczyna się dopiero w temperaturze o koło 10 K wyższej (patrz odpowiednia krzywa TGA/DSC). Wraz z utratą masy na krzywej TGA/DSC pojawia się również ramię podobne do obserwowanego w pomiarze DSC (patrz rysunek 4). Przy 10 K/min rozkład również rozpoczyna się wcześniej niż topnienie. W przeciwieństwie do pomiarów DSC początek rozkładu nie jest już wyraźnie widoczny jako ramię na krzywej TGA/DSC. Punkty topnienia (onset) wyznaczone z krzywych TGA/DSC zgadzają się dobrze z wartościami ocenionymi na podstawie krzywych DSC.
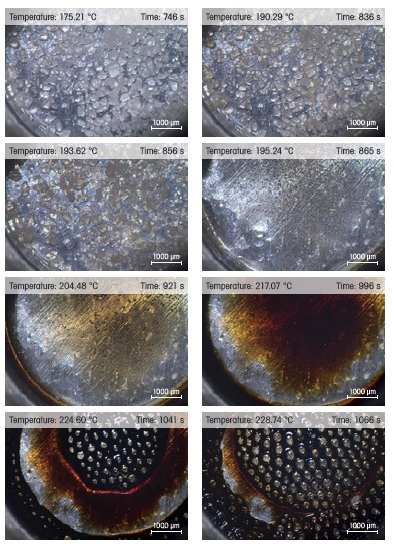
Rysunek 3. Obrazy próbki witaminy C w wybranych temperaturach.
Wnioski
Punkty topnienia (onset) wielu czystych krystalicznych związków organicznych stosowanych w branżach
spożywczej i farmaceutycznej są niższe przy niskich szybkościach ogrzewania niż przy wysokich. Poza tym kształt piku topnienia jest inny niż oczekiwany dla czystych materiałów (przepływ ciepła czystych substancji rośnie liniowo podczas topnienia).

Rysunek 4. Przebieg topnienia witaminy C zmierzony przy różnych szybkościach ogrzewania w statycznym powietrzu.

Rysunek 5. Zależność temperatury onset piku topnienia (niebieska krzywa) i temperatury piku rozkładu (czerwona krzywa) witaminy C od szybkości ogrzewania na podstawie pomiarów DSC. Oś x jest w skali logarytmicznej.
Powodem takiego zachowania jest fakt, że rozkład materiału rozpoczyna się tuż przed topnieniem lub w tym samym czasie. Przy niskich szybkościach ogrzewania na jeden przyrost temperatury przypada więcej czasu, w którym mogą zachodzić takie procesy. Stężenie zanieczyszczeń powstających w wyniku rozkładu wzrasta zatem wraz z malejącą szybkością ogrzewania, co prowadzi do obniżenia temperatury topnienia. W takich przypadkach ogrzewanie musi następować bardzo szybko, aby określić „prawdziwą” temperaturę topnienia czystego produktu. Rozkład przenosi się wówczas do wyższych temperatur, co pozwala określić temperaturę topnienia czystej substancji. W przypadku witaminy C szybkości ogrzewania większe niż 50 K /min wystarczają do przesunięcia rozkładu w zakres temperatur powyżej temperatury topnienia. Przy tak dużych szybkościach ogrzewania zalecamy stosowanie aluminiowego tygla o pojemności 20 μl lub nawet pokrywki aluminiowego tygla o pojemności 20 μl jako tygla (w takim przypadku nie można używać podajnika próbek). Pozwala to znacznie skrócić stałą czasową sygnału w porównaniu ze stałą czasową standardowego tygla aluminiowego o pojemności 40 μl. Ponadto przy tak dużych szybkościach ogrzewania masy próbek mniejsze niż 1 mg są całkowicie wystarczające do zbadania przebiegu topnienia. Przy dużych szybkościach ogrzewania zalecamy zmniejszenie odstępu próbkowania sygnału DSC do 0,02 s (domyślne ustawienie to 1 s). Jeśli szybkość ogrzewania DSC nie będzie wystarczająco duża, aby przesunąć rozkład do temperatury powyżej temperatury topnienia, to oczywiście pomiar można przeprowadzić za pomocą urządzenia Flash DSC
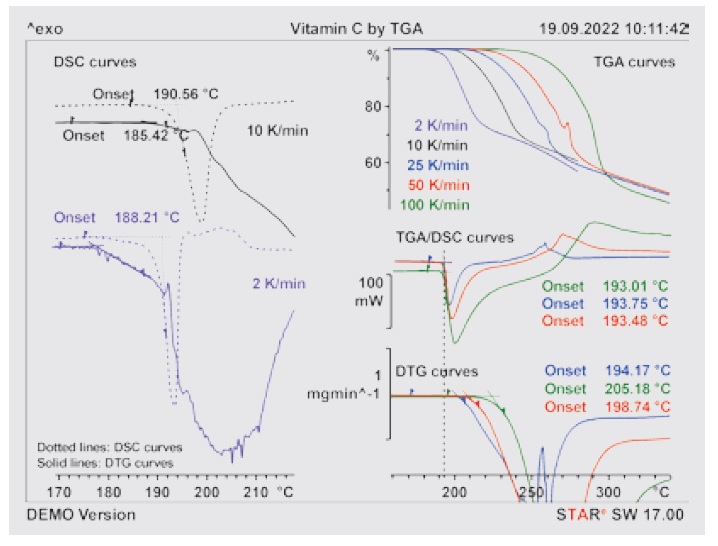
Rysunek 6. Krzywe TGA, DTG i DSC z pomiarów TGA/DSC przy 2, 10, 25, 50 i 100 K/min w powietrzu o prędkości przepływu 30 ml/min. Masa próbki wynosiła około 5,5 mg.
Literatura
[1] Y. Corvis, Ph. Espeau, A. Wurm, Ch. Schick, Determination of the glass transition temperature of difficult samples by Flash DSC, UserCom 45, 15–17.
